[云南]2011-2012学年云南蒙自高中高二上学期期中考试化学试卷
下列对化学反应的认识错误的是( )
| A.会引起化学键的变化 | B.会产生新的物质 |
| C.必然引起物质状态的变化 | D.必然伴随着能量的变化 |
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片与稀H2SO4反应 | B.Ba(OH)2·与NH4Cl反应 |
| C.灼热的炭与CO2反应 | D.甲烷在O2中燃烧反应 |
下列与化学反应能量变化相关的叙述正确的是 ( )
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+ Cl2(g) = 2HCl(g)在光照和点燃条件下的△H不同 |
对于化学反应3W(g)+ 2X(g)= 4Y(g) + 3Z(g),下列反应速率关系中,正确的是( )
| A.V(W)=3V(Z) | B.2V(X)= V(Y) |
| C.2V(X)= 3V(Z) | D.3V(W) = 2V(X) |
在N2+3H2 = 2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6mol/L,在此段时间内用H2表示的平均反应速率为0.45mol/(Ls),此段时间是 ( )
| A.1s | B.2s | C.44s | D.1.33s |
对于反应2SO2 + O2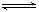 2SO3,下列变化可增大活化分子百分数而使反应速率加快的是( )
2SO3,下列变化可增大活化分子百分数而使反应速率加快的是( )
下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
在密闭容器中进行如下反应:H2(g) +I2(g) 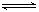 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是( )
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是( )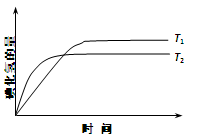
| A.T1>T2,ΔH>0 | B.T1>T2,ΔH<0 |
| C.T1<T2,ΔH>0 | D.T1<T2,ΔH<0 |
下列说法正确的是 ( )
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
| B.自发反应一定熵增大,非自发反应一定是熵减少或不变 |
| C.熵增加且放热的反应一定是自发反应 |
| D.非自发反应在任何条件下都不能实现 |
等体积、等物质的量浓度的盐酸和醋酸比较,下列说法错误的是:( )
| A.溶液中pH盐酸比醋酸大 |
| B.与足量的锌粉反应产生的氢气体积相同 |
| C.与足量锌粒反应时,一开始盐酸的速率快 |
| D.中和NaOH溶液的能力相同 |
下图是关于反应A2(g)+3B2(g) 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
下列溶液一定呈中性的是( )
| A.pH=7的溶液 |
| B.c(H+)=c(OH—)的溶液 |
| C.由强酸、强碱等物质的量反应得到的溶液 |
| D.非电解质溶于水得到的溶液 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A.HClO | B.Na | C.C2H5OH | D.SO2 |
已知0.1 mol/L的氨水溶液中存在电离平衡:NH3·H2O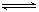 NH4++OH—,要使溶液中c(OH—)/c(NH3·H2O)值增大,可以采取的措施是( )
NH4++OH—,要使溶液中c(OH—)/c(NH3·H2O)值增大,可以采取的措施是( )
| A.加少量盐酸溶液 | B.加入少量NH4Cl晶体 |
| C.加少量NH3 | D.加水 |
反应热是指 ( )
| A.热化学方程式中标注的“±a kJ·mol—1” |
| B.特指1mol反应物燃烧时放出的热量 |
| C.不论多少物质反应放出的热量都是反应热 |
| D.专指化学反应过程中放出的热量 |
决定化学反应速率的主要因素是 ( )
| A.反应物的浓度 | B.外界的压强 |
| C.催化剂 | D.反应物的性质 |
25℃的下列溶液中,碱性最强的是 ( )
| A.pH = 11的溶液 | B.c(OH-) =" 0.12" mol/L的溶液 |
| C.1L中含有4 g NaOH的溶液 | D.c(H+) = 1×10-10 mol/L的溶液 |
下列叙述中,能证明某物质是弱电解质的是 ( )
| A.熔化时不导电 |
| B.水溶液的导电能力很差 |
| C.溶液中已电离的离子和未电离的分子共存 |
| D.不是离子化合物,而是共价化合物 |
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡移动的是( )
| A.反应混和物的浓度 | B.正、逆反应速率 |
C.反应混和物的压强 | D.反应混合物中各物质的百分含量 |
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A、均减半 B、均加倍 C、均增加0.5mol D、均减少0.5mol
已知:HCN(aq)与NaOH(aq)反应的ΔH ="-15.1" kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH ="-55.6" kJ·mol-1,则HCN在水溶液中电离的ΔH等于( )
| A.+53.7 kJ·mol-1 | B.+40.5 kJ·mol-1 |
| C.+43.5 kJ·mol-1 | D.+70.7kJ·mol-1 |
醋酸水溶液中的PH为2时,该溶液中C(OH—)是 ( )
| A.1×10-7 mol·L-1 | B.1×10-2mol·L-1 |
| C.1×10-14 mol·L-1 | D.1×10-12 mol·L-1 |
下列事实不能用勒夏特列原理解释的是 ( )
| A.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| B.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
| C.在含有Fe(SCN)3的红色溶液中加入铁粉,振荡静置, |
| D.氨水应密闭保存,置低温处 |
在一定真空密闭容器中盛有1mol PCl5,加热到200℃,发生反应:PCl5(g) PCl3(g)+Cl2(g),反应达到平衡时,PCl3在混合气体中的体积分数为m%,保持温度和容积不变,再加入1mol PCl5,反应达到平衡时,PCl3在混合气体中的体积分数为n%,则m和n的关系正确的是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl3在混合气体中的体积分数为m%,保持温度和容积不变,再加入1mol PCl5,反应达到平衡时,PCl3在混合气体中的体积分数为n%,则m和n的关系正确的是( )
| A.m > n | B.m < n |
| C.m = n | D.无法比较 |
根据强弱电解质的概念回答下列问题: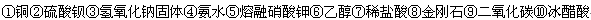
其中能够导电的是 ;属于强电解质的是 ;属于弱电解质的是 ;属于非电解质的是 (注回答不全不给分)
、根据电离平衡移动原理完成下列表格
(1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况
| 外加条件 |
平衡移动方向 |
C(OH -) |
C(CH3COO -) |
| 升温 |
|
不填 |
不填 |
| 加水 |
|
|
不填 |
| 加盐酸 |
不填 |
|
|
| 加少量氢氧化钠固体 |
不填 |
不填 |
|
(2)在一定温度下,冰醋酸加水稀释过中溶液的导电能力如下图所示,请回答: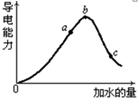
①写出醋酸的电离方程式________________。
②a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
③a、b、c三点中醋酸的电离程度最大的是 。
④取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲_____ 10C(H+)乙(填“大于”、“小于”或 “等于”),
(1)①根据图示,写出反应的热化学方程式: 。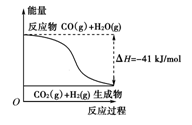
②根据如图所示情况,判断下列说法中正确的是( )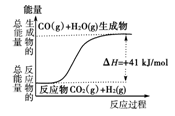
| A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41 kJ/mol |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
| D.当H2O为液态时,其反应热值小于41 kJ/mol |
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是 。
(3)如图是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为: 。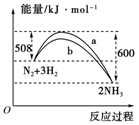
a、b两条曲线产生区别的原因很可能是 。
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示 , K值大小与温度的关系是:温度升高,K值_________________。(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=_________mol·L-1·min-1。
CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=_________mol·L-1·min-1。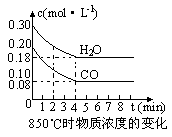
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。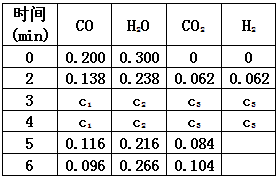
①表中3min~4min之间反应处于_________状态;
c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________ (单选),表中5min~6min之间数值发生变化,可能的原因是_________ (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
高炉炼铁过程中发生的主要反应为:
1/3Fe2O3(s)+CO(g) 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下: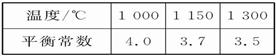
请回答下列问题:
(1)该反应的平衡常数表达式K=_____,ΔH____0(填“>”、“<”或“=”);
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平衡反应速率v(CO2)=_____、CO的平衡转化率=_____;
某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g) cC(g)表示]化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):
cC(g)表示]化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):
分析图像,回答下列问题:
(1)在图像反应Ⅰ中,若P1<P2(填“>”、“<”或“=”),则此正反应为是一个气体分子数_____(填“减少”或“增大”)的反应,该正反应为_____(填“吸热”或“放热”)反应。由此判断,此反应自发进行的温度是__ ___。(填“低温”“高温”“任何温度”)
(2)在图像反应Ⅱ中,T1_____T2(填“>”、“<”或“=”),该正反应为_____(填“吸热”或“放热”)反应。
(3)在图像反应Ⅲ中,若T1>T2,该反应能否自发进行
 粤公网安备 44130202000953号
粤公网安备 44130202000953号