2010年全国中考真题专题汇编专题六 化学方程式计算(一)
(10滨州26).钙是维持人体正常功能所必需的元素。右图所示为某种补钙剂“钙尔奇”说明书的一部分。取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应)。烧杯内物质质量变为11.34g。
试计算:
(1)每片钙尔奇中含碳酸钙的质量。
(2)服用这种补钙剂,每人每天摄入钙元素的质量。
(3)所用稀盐酸中溶质的质量分数。
(10眉山24)、实验室常用锌块和稀盐酸反应制取氢气,若用2.6克锌和稀盐酸反应。则:
(1)可制取多少克氢气?
(2)理论上需要质量分数为14.6﹪的稀盐酸溶液多少克?
(10安徽16).(6分)向50.0g 8.O%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时溶液pH=7.
(1)求反应前氢氧化钠溶液中溶质的质量
(2)求反应后生成硫酸钠的质量。
(10重庆24).上海世博会上,100辆燃料电池观光车活跃在世博园区,它们靠氢气和氧气反应提供能量。由于它们“喝”的是氢气,产生的是水,真正实现了“零排放”。
⑴若燃烧1kg氢气,需氧气多少千克?
⑵在燃料电池里需要加入30%的KOH溶液。现有10kg 10%的KOH溶液、14kg KOH固体和适量蒸馏水,可以配制出30%的KOH溶液多少千克?
(10芜湖16).发射通信卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染。
(1)反应的化学方程式为2N2H4+N2O4=3 +4H2O,请在横线上填写化学式以完成该化学方程式。
(2)请计算9.6gN2H4完全燃烧需要助燃物的质量。
(10潼南24).10克碳酸钙与稀盐酸反应的关系如右图。
⑴当加入73克稀盐酸时,稀盐酸与碳酸钙恰好完全反应。
① 当加入73克稀盐酸时,反应生成的气体的质量是多少?
② 当加入73克稀盐酸时,反应后溶液中溶质的质量分数是多少?
⑵当加入120克稀盐酸时,溶液中溶质是 。
(10潍坊24).(10分)碳酸氢钠(NaHCO3)俗称小苏打,是一种白色固体,是焙制糕点所用的发酵粉的主要成分之一,它能与稀硫酸等酸反应生成CO2。试回答:
(1) 写出NaHCO3与稀硫酸反应的化学方程式 。
(2)如何用98%的硫酸(密度为1.849/mL)配制980918.4%的硫酸溶液?
。
(3)现将45g NaHCO3(混有KHCO3)固体粉末加入100mL稀硫酸,恰好完全反应后使气体全部逸出,固体粉末的质量与产生CO2体积的关系如图(该状况下,CO2的密度为2g/L)。通过计算:
①求100mL稀硫酸中硫酸的质量。
②若稀硫酸为120mL时,加入固体粉末为58.5g,求产生CO2的体积。
(10昆明30)(2)蒸馒头用的某纯碱中含有少量的氯化钠,为了测定该纯碱中碳酸钠和氯化钠的含量,取一定量的该纯碱样品全部溶解在100g水中,再加入氯化钙141g,恰好完全反应。(反应方程式为Na2CO3+CaCl2====CaCO3+2NaCl)经过滤、干燥后称得沉淀质量为10g,所得滤液中氯化钠的质量分数为5%,请计算:
①纯碱样品中碳酸钠的质量;
②纯碱样品中氯化钠的质量。
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:
| |
第1次 |
第2次 |
第3次 |
第4次 |
| 加人稀硫酸质量(g) |
100 |
100 |
100 |
100 |
| 剩余固体质量(g) |
87 |
74 |
67.5 |
67.5 |
(1)第2次测得剩余固体质量为74g,其成分为 ▲ 。
A.铜 B.锌 C.铜和锌
(2)该黄铜样品中铜和锌的质量比m铜:m锌: ▲ 。
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图。
晴晴同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石灰石样品中逐滴加人稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g。试计算:
(1)碳酸钙中钙元素的质量分数是多少?
(2)该石灰石样品中碳酸钙的质量分数为多少?(写出计算过程,结果精确至0.1%)
(3)若要计算上述反应所消耗盐酸溶液的质量,题中还缺少的一个数据是。
____________________________________________。
电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点
是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:
PbO2 (固)+ 2H2SO4 + Pb = 2PbSO4 ↓+ 2H2O
当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1)电瓶在放电时, ▲ 能转化为电能。
(2)假如某个电瓶中铅的质量为1800克,内装36%的稀硫酸1200克,当有310.5克的铅参加反应时,需消耗稀硫酸中溶质多少克?此时电瓶中硫酸溶液溶质的质量分数是多少?
(最后结果保留两位小数)
对化肥的销售,国家规定了明确的质量要求。某农业科技人员对农民买来的钾肥进行了检测,称取4.0g样品放入小烧杯中,加入适量的水溶解后,与足量氢氧化钡溶液充分反应。产生沉淀的质量与所加入的氢氧化钡溶液质量的关系如图所示。(假定杂质不参加反应,反应方程式为K2SO4+Ba(OH)2=BaSO4↓+2KOH)通过计算钾肥中硫酸钾的质量分数判断该产品是否符合包装说明?
| XX牌钾肥 主要成分:K2SO4((K2SO4含量≥86%) 净重: 50Kg XX化工有限公司 |

(10宽甸)23.为了测定某些磁铁矿中四氧化三铁的质量,甲、乙两组同学根据磁铁矿与一氧化碳反应的原理,分别利用两种方法测定了磁铁矿样品中四氧化三铁的质量分数。已知磁铁铁矿与一氧化碳反应的化学方程式如下(假设磁铁矿中的杂质不参加反应):Fe3O4+4CO  3Fe + 4CO2。(计算最终结果保留小数点后一位)
3Fe + 4CO2。(计算最终结果保留小数点后一位)
(1)甲组同学取该磁铁样品10g,与足量的一氧化碳充分反应,并将产生的气体通入足量的氢氧化钠的溶液中,溶液的质量增加了5.5g。请你根据甲组同学的实验数据,计算出磁铁矿样品中四氧化三铁的质量分数。
(2)乙组同学取该磁铁样品10g,与足量的一氧化碳充分反应,测得反应后固体物质的质量为8g。请你根据乙组同学的实验数据,计算出磁铁矿样品中四氧化三铁的质量分数。
38.硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空气大,可溶于水形成氢硫酸,氢硫酸具有酸的通性。实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04。
(1)在右图中,应选用图 作为制取H2S的装置。
(2)收集H2S气体时,应从C装置中的 导管进入,对产生尾气的处理方法
是: 。
(3)实验室若制取6.8克的硫化氢气体,理论上需要多少克20%的硫酸溶液?
.科学家发现,海底可燃冰分布的范围约占海洋总面积的10%,其储量是 煤、石油和天然气总和的两倍,是迄今为止发现的海底最具价值的矿产
资源。可燃冰也称为“甲烷水合物”。“置换法”是开采可燃冰设想方案之一,即将CO2注人海底的甲烷水合物储层,CO2较甲烷更易形成水合物,因而就能将甲烷水合物中的甲烷分子“挤走”,从而将其“置换”出来(原理:CH4·nH2O+CO2==CO2·nH2O+CH4)。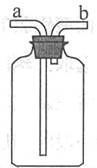
(1)通常情况下,CH4是一种无色、无味、难溶于水、密度比空气小的气体。用如图所示的
装置收集CH4气体时,则应让气体从 (选填“a”或“b”)管通入。
(2)若上述方法能够实现,那么要制取8吨的CH4气体,理论上需CO2多少吨?
.在氢气还原氧化铜的实验中,向50克氧化铜粉末中通氢气,加热一段时间后,测得固体质量减少8g,求:
(1)已反应掉的氧化铜质量。(列式计算)
(2)若实验时用的氢气,是用右图标签所示的浓硫酸稀释成稀硫酸后和足量的锌粒反应制取的。取用浓 硫酸50毫升,小心加入到300毫升水中稀释,稀释后硫酸溶液的溶质质量分数为 。
.下图是用铜粉氧化法生产氧化铜的流程图。据图回答下列问题:
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质。氧化亚铜(Cu2O)中铜元素的化合价是________价。
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜。假如固体1中只含有铜的氧化物,下列推理合理的是___________(填序号)。
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)将得到的1.6吨氧化铜全部转化为硫酸铜,可得硫酸铜多少吨?(CuO+H2SO4=CuS04+H2O)
(4)若用贴有如图标签的浓硫酸100毫升可配制溶质质量分数为49%的硫酸溶液_____克。
.构建知识网络是一种重要的学习方法。图为某同学绘制的铁的化学性质网络示意图。请分析回答下列问题:
(1)反应①中可用 ▲ (填化学式)作还原剂;
(2)反应②导致每年有大量的钢铁锈蚀,为阻止该反应的发生,人们常采用在钢铁表面涂刷油漆或镀上其它金属等方法。这两种方法的共同原理是阻止钢铁与 ▲ 接触;
(3)早在西汉时期,我国劳动人民就利用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”,即反应③,若用该方法制得铜16千克,理论上需要溶质质量分数为10%的硫酸铜溶液多少千克?
(10广东省25)氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气和氢
氧化钠等物质,发生的化学反应如下:2NaCl + 2H2O Cl2 ↑+ H2 ↑+ 2NaOH。现取100g
Cl2 ↑+ H2 ↑+ 2NaOH。现取100g
的溶质质量分数为25%的氯化钠溶液进行电解,一段时间后停止通电,生成氯气的质量7.1g。
请计算:
(1)生成氢气的质量是多少?剩余氯化钠的质量是多少?
(2)反应后溶液中NaOH的质量分数是多少?
(10四川达州14)50g溶质质量分数为7.3%的稀盐酸与50g一定溶质质量分数的氢氧化钠溶液恰好完全反应,求反应后所得溶液溶质质量分数。
(10重庆綦江24)小青同学为了制作叶脉书签,打算配制125g10%的NaOH溶液。
(l)计算小青需要称取NaOH的质量。
(2)小青将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少了5g,溶质质量分数也有所减小。为了侧定剩下溶液中NaOH的质量分数,小青向溶液中逐渐加入7.3%的稀盐酸,当溶液PH=7时,消耗盐酸50g。计算:
①生成NaCl的质量。
②剩下溶液中NaOH的质量分数。
(10鄂州)23.某工厂需要200kg氢气制备高纯度硅。若用电解水的方法制取这些氢气,需消耗水的质量是多少?(2H2O 2H2↑+O2↑)
2H2↑+O2↑)
(10重庆江津24)钙是人体中含量较高的常量元素之一,缺钙可能导致幼儿及青少年发育不良,严重时还会患佝偻病。李明的父亲为他买回一瓶补钙保健品,他仔细阅读了标签上的说明(如图)。为了验证该保健品中碳酸钙的含量,取出5片药品,加入足量的稀盐酸,充分反应后收集到3.3g二氧化碳(假定除碳酸钙外,其他成分不与盐酸反应)
(1)已知碳酸钙的相对分子质量是100,则钙元素的相对原子质量为____________。
(2)通过计算验证:该保健品主要原料含量是否属实(写出计算过程)?
(3)李明按照说明服用一个月(30天),理论上吸收了钙元素_____克。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号