2022年江苏省镇江市中考化学试卷
下列物质的用途主要与化学性质有关的是( )
| A. |
用金刚石切割玻璃 |
B. |
用液氮作医疗冷冻剂 |
| C. |
用水银制作温度计 |
D. |
用酒精作实验室燃料 |
下列做法不符合“健康、安全、绿色、舒适”生活理念的是( )
| A. |
海鲜防腐,甲醛浸泡 |
B. |
油锅着火,锅盖盖灭 |
| C. |
垃圾分类,资源再生 |
D. |
限放鞭炮,保护环境 |
下列归类正确的是( )
|
选项 |
归类 |
内容 |
|
A |
合成材料 |
塑料、橡胶、玻璃钢 |
|
B |
碱性溶液 |
氨水、雨水、肥皂水 |
|
C |
营养物质 |
糖类、油脂、蛋白质 |
|
D |
复合肥料 |
碳铵、尿素、硝酸钾 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
用浓硫酸配制一定浓度的稀硫酸并制取氢气,下列实验操作不正确的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
下列实验方法正确的是( )
| A. |
用活性炭软化硬水 |
| B. |
用水区分 |
| C. |
加热蒸发碳酸氢铵溶液获得其晶体 |
| D. |
用灼烧的方法除去铜粉中的炭粉 |
下列指定反应的化学方程式正确的是( )
| A. |
天然气燃烧: |
| B. |
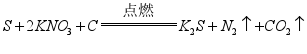
黑火药爆炸: |
| C. |
铜绿的形成: |
| D. |
工业上用石灰乳吸收 |
某冶炼厂处理尾气时有下列转化。
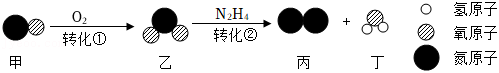
下列说法不正确的是( )
| A. |
转化①是化合反应 |
| B. |
转化过程中N的化合价有三种 |
| C. |
整个转化中,甲与丙的分子个数之比为 |
| D. |
该处理能减少硝酸型酸雨的形成 |
甲醇燃料电池的反应为 。下列说法不正确的是( )
。下列说法不正确的是( )
| A. |
该反应中有三种氧化物 |
| B. |
|
| C. |
|
| D. |
相比燃烧发电,该反应将化学能转化为电能的效率高 |
 固体不溶于水,用如图装置研究
固体不溶于水,用如图装置研究 受热分解产物。下列说法不正确的是( )
受热分解产物。下列说法不正确的是( )

A.实验时,先加热 ,后加热
,后加热
B.装置②中黑色固体变红,说明分解产物中有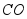
C.装置③中澄清石灰水变浑浊,说明分解产物中有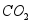
D.冷却后,取装置①中少量残留固体加入水,无气泡,放热,证明有 生成
生成
下列实验操作能达到实验目的的是( )
|
选项 |
物质 |
目的 |
主要实验操作 |
|
A |
蚕丝、羊毛线 |
鉴别 |
取样,灼烧,闻气味 |
|
B |
|
分离 |
溶解、过滤、洗涤、烘干,蒸发结晶 |
|
C |
与 |
检验 |
取样,滴加 |
|
D |
|
除杂 |
加入过量的 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
一种新型合成氨的方法如图所示( 是一种金属)。下列说法不正确的是( )
是一种金属)。下列说法不正确的是( )

| A. |
反应①中电能转化为化学能 |
| B. |
反应③为 |
| C. |
理论上,整个转化过程无需补充水 |
| D. |
理论上,合成 |
下列说法正确的是( )
| A. |
洗洁精和汽油均可清洗油污,其原理相同 |
| B. |
食盐水能导电是因为溶液中含有较多自由移动的离子 |
| C. |
向鸡蛋清溶液中加入乙酸铅溶液,产生固体,加水,固体溶解 |
| D. |
将燃着的镁条伸入某气体中,镁条继续燃烧,该气体中一定含氧气 |
如图为 和
和 的溶解度曲线。下列说法正确的是( )
的溶解度曲线。下列说法正确的是( )

| A. |
|
| B. |
将 |
| C. |
将 |
| D. |
将等质量的两物质饱和溶液从 |
向盛有 和
和 混合溶液的烧杯中,加入过量
混合溶液的烧杯中,加入过量 溶液,充分反应后再滴加溶质质量分数为20.0%的
溶液,充分反应后再滴加溶质质量分数为20.0%的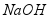 溶液,烧杯中沉淀质量与滴加
溶液,烧杯中沉淀质量与滴加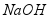 溶液质量的关系如图所示。下列说法正确的是( )
溶液质量的关系如图所示。下列说法正确的是( )

| A. |
加入 |
| B. |
|
| C. |
原混合溶液中 |
| D. |
取a点对应溶液,滴加稀 |
已知: ,
, 。现将一定质量的
。现将一定质量的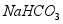 、
、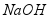 固体混合物,在密闭容器中加热至固体质量不再改变,剩余15.9g固体。将生成的气体全部通入足量澄清石灰水中,产生10.0g沉淀。下列说法正确的是( )
固体混合物,在密闭容器中加热至固体质量不再改变,剩余15.9g固体。将生成的气体全部通入足量澄清石灰水中,产生10.0g沉淀。下列说法正确的是( )
A.剩余固体为混合物
B.原固体加热共生成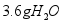
C.原混合物中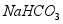 和
和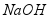 的质量比为
的质量比为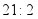
D.取两份等质量的原混合物,一份直接与盐酸反应,另一份加热后再与盐酸反应,消耗 的质量不相等
的质量不相等
用化学符号表示。
(1)磷元素 ;
(2)人体中含量最高的物质 ;
(3)2个铁离子 ;
(4)人体中 元素缺少或过量,均会导致甲状腺疾病。
选择下列适当的物质填空(选填序号)。
A.干冰B.食盐C.石灰石D.苛性钠E.盐酸F.明矾G.熟石灰H.维生素
(1)可用于人工降雨的是 ;
(2)常作净水混凝剂的是 ;
(3)可用于金属除锈的是 ;
(4)可改良酸性土壤的是 ;
(5)厨房中作调味品的是 ;
(6)工业炼铁所需原料是 。
取一根小木条,一端蘸有硫粉,进行如图所示实验。

(1)点燃,生成的气体有 、
、 和 (填化学式)。
和 (填化学式)。
(2)振荡烧杯A,可观察到 的现象。
民以食为天,人类主要通过食用淀粉获得能量。
(1)大米、面粉等食物中的淀粉是绿色植物通过 合成、转化形成的。
(2)2021年9月,中国科学家发表了利用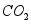 、
、 人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少
人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少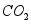 排放,缓解 (填环境问题)等。
排放,缓解 (填环境问题)等。
(3)如图为人工合成淀粉的关键步骤。

①图中转化Ⅰ的化学方程式为 。
②经检测,人工合成的淀粉与天然淀粉在分子组成、结构上一致,实验室可用 初步检验出有淀粉生成。
(4)获得大量 是人工合成淀粉的重要一步。如图是制氢、贮氢与释氢的一种方法。
是人工合成淀粉的重要一步。如图是制氢、贮氢与释氢的一种方法。
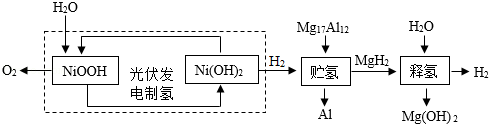
①虚线框内制氢的总反应化学方程式为 。
②释氢释放的 比贮氢吸收的
比贮氢吸收的 (选填“多”或“少”)。
(选填“多”或“少”)。
用某废渣(含 、
、 和
和 )制备碳酸镁晶体的流程如下。
)制备碳酸镁晶体的流程如下。
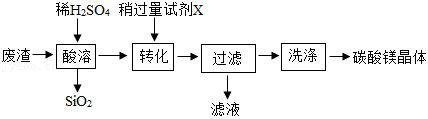
(1)试剂X应选用 (选填序号)。
| A. |
a. |
| B. |
b. |
| C. |
c. |
(2)过滤用到的玻璃仪器有 、烧杯、玻璃棒、胶头滴管等。
(3)洗涤时检验晶体已洗净的方法:取最后一次洗涤后的滤液,先滴加稀盐酸,再滴加 (填化学式)溶液,无现象。
(4)若加入试剂X过多,制得的碳酸镁晶体中会含有较多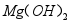 ,原因是 。
,原因是 。
如图,向 溶液中滴加
溶液中滴加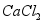 溶液,并测定溶液pH,观察到溶液变浑浊且出现气泡,澄清石灰水变浑浊。
溶液,并测定溶液pH,观察到溶液变浑浊且出现气泡,澄清石灰水变浑浊。
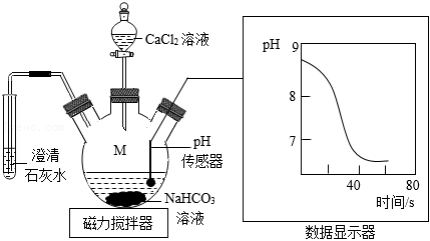
(1)仪器M中发生反应的化学方程式为 。
(2)已知: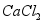 溶液呈中性,最终溶液呈酸性的原因 。
溶液呈中性,最终溶液呈酸性的原因 。
结合如图回答问题。
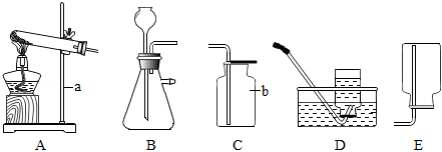
(1)仪器名称:a ,b 。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置 (选填序号)和D组合,反应的化学方程式为 ,二氧化锰的作用是 。
(3)用如图装置制取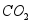 并验证相关性质。
并验证相关性质。
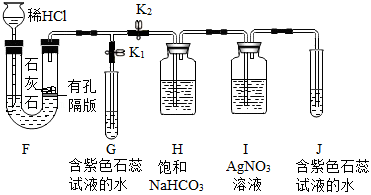
①装置F中发生反应的化学方程式为 。
②装置F相对于装置B的优点是 。
③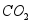 可用装置C收集,原因是 。
可用装置C收集,原因是 。
④关闭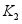 ,打开
,打开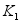 ,装置G中溶液变红;关闭
,装置G中溶液变红;关闭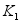 ,打开
,打开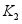 ,装置J中溶液变红。将变红的两溶液加热相同时间,装置J中溶液变成紫色,而装置G中溶液仍显红色。
,装置J中溶液变红。将变红的两溶液加热相同时间,装置J中溶液变成紫色,而装置G中溶液仍显红色。
Ⅰ.装置G中溶液仍显红色的原因是 。
Ⅱ.装置Ⅰ的作用是 。
用下列实验探究 与
与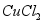 溶液的反应。
溶液的反应。
实验一:将打磨后的铝片插入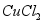 溶液,铝片表面出现红色固体且产生气泡,最终溶液呈无色。
溶液,铝片表面出现红色固体且产生气泡,最终溶液呈无色。
(1)生成红色固体的化学方程式为 。
(2)收集气体, (填操作)后点燃,产生淡蓝色火焰。该气体为 。
实验二:将实验一所得无色溶液倒入水中,出现白色固体。过滤、洗涤,低温烘干。对所得白色固体作如下探究。
【资料】①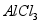 能与
能与 作用生成
作用生成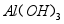 。
。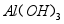 ,白色固体,不溶于水,受热易分解生成
,白色固体,不溶于水,受热易分解生成 和
和 。
。
② 与
与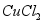 溶液反应会生成
溶液反应会生成 。
。 ,白色固体,不溶于水,能溶于含
,白色固体,不溶于水,能溶于含 浓度较大的溶液,受热不分解。
浓度较大的溶液,受热不分解。
【猜测】白色固体可能是:
a. 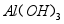 ;b.
;b.  ;C.
;C. 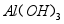 和
和 。
。
【实验】取适量白色固体,利用如图装置充分加热,U型管中 ,则猜测b成立。
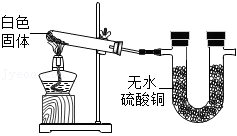
【反思】无色溶液倒入水中后出现白色固体的原因是 。
实验三: 在空气中被氧化成碱式氯化铜[
在空气中被氧化成碱式氯化铜[ ]蓝绿色固体,其受热会分解生成
]蓝绿色固体,其受热会分解生成 、
、 和
和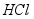 。取一定量蓝绿色固体,充分加热,将生成的气体依次用足量的吸水剂氯化钙和烧碱溶液充分吸收。
。取一定量蓝绿色固体,充分加热,将生成的气体依次用足量的吸水剂氯化钙和烧碱溶液充分吸收。
(1)实验测得氯化钙增重0.36g,烧碱溶液增重0.73g。则碱式氯化铜的化学式为 。
(2)若烧碱溶液吸收了空气中的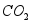 ,则测得的
,则测得的 中
中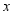 值 (选填“偏大”、“偏小”或“不变”)。
值 (选填“偏大”、“偏小”或“不变”)。
现有一包不纯的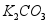 固体,可能含有
固体,可能含有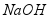 、
、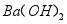 、
、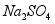 、
、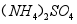 中的一种或几种。现做如下实验。
中的一种或几种。现做如下实验。
(1)取适量固体与熟石灰混合研磨,无氨味,则原固体一定不含 。
(2)另取适量固体加水溶解,过滤得白色固体A和无色滤液B,则原固体中一定含 。
(3)取固体A,加入过量稀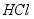 ,固体全部溶解,则原固体中一定不含 ,写出步骤(2)中生成固体A的化学方程式 。
,固体全部溶解,则原固体中一定不含 ,写出步骤(2)中生成固体A的化学方程式 。
(4)取少量滤液B,滴加足量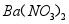 溶液,产生沉淀,静置,向上层清液滴加酚酞试液,溶液变红,则原固体中 (选填“一定”或“不一定”)含
溶液,产生沉淀,静置,向上层清液滴加酚酞试液,溶液变红,则原固体中 (选填“一定”或“不一定”)含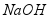 。
。
从古至今,铁及其化合物一直被人类广泛应用。
(一)铁及其化合物的应用

(1)明代科学著作《天工开物》中记载:
①“其器冶铁锥,其尖使极刚利”,“铁锥”为开挖盐井的工具。所取盐井水“入于釜中煎炼顷刻结盐”,“金”指生铁制作的铁锅。生铁属于 材料。上述描述中利用铁的 (选填序号)。
| A. |
a.导热性 |
| B. |
b.导电性 |
| C. |
c.硬度大 |
②“泥固塞其孔,然后使水转釉”是指高温下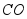 将红砖中的
将红砖中的 转化为
转化为 而形成青砖。该转化的化学方程式为 。
而形成青砖。该转化的化学方程式为 。
(2)铁的化合物在现代更多领域发挥着重要作用。
①碳酸亚铁( )不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
)不溶于水,可作补血剂,服用后与胃酸反应生成 被人体吸收,促进血红蛋白的生成。
②火星探测器发回的信息表明,火星上存在 ,从而证明火星表面曾经存在过水,其理由为 。
,从而证明火星表面曾经存在过水,其理由为 。
③活性 可除去石油开采过程中的有害气体
可除去石油开采过程中的有害气体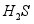 ,并获得
,并获得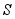 ,原理如下。
,原理如下。
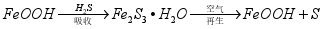
吸收中生成的另一种物质的化学式为 ,再生时发生反应的化学方程式为 。
(二) 的制备
的制备
用废铁屑(主要成分为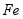 ,含少量
,含少量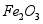 和
和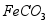 )制备
)制备 主要流程如下。
主要流程如下。
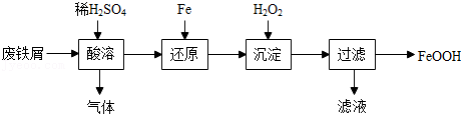
(1)酸溶时适当提高反应温度和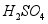 浓度,目的是 ,产生的气体为 。
浓度,目的是 ,产生的气体为 。
(2)还原发生的反应为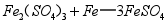 。
。
沉淀发生的反应为 。
。
沉淀时反应温度不宜太高,原因是 。
(3)沉淀时会有部分 与
与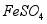 反应生成
反应生成 ,反应的化学方程式为 。
,反应的化学方程式为 。
(三) 的含量测定
的含量测定
已知: 及铁的氧化物加热分解的温度如下。
及铁的氧化物加热分解的温度如下。

称取含 的
的 样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。
样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图所示。
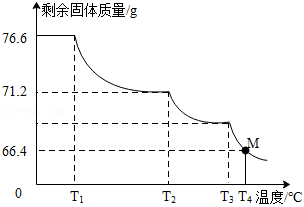
(1)样品中 的含量为 %(精确到0.1%)。
的含量为 %(精确到0.1%)。
(2)当加热到 时,M点固体的成分是 ,对应的质量比为 。
时,M点固体的成分是 ,对应的质量比为 。
 量取
量取 稀释
稀释 产生
产生
 收集
收集
 固体
固体





 :
: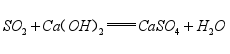

 为侯氏制碱法中的碱
为侯氏制碱法中的碱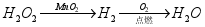
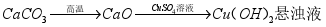


 粉末
粉末 溶液,观察有无沉淀
溶液,观察有无沉淀 溶液中混有
溶液中混有
 ,同时得到
,同时得到
 时,将
时,将 固体加到50g水中,所得溶液的溶质质量分数为37.5%
固体加到50g水中,所得溶液的溶质质量分数为37.5% 升温到
升温到 ,溶质质量分数变大
,溶质质量分数变大 饱和溶液从
饱和溶液从 ,析出
,析出 晶体
晶体 、
、 、
、 、
、
 、
、
 、
、 、
、
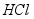 、
、
 与
与
 悬浊液
悬浊液 粤公网安备 44130202000953号
粤公网安备 44130202000953号