2017年江苏省镇江市中考化学试卷
下列归类错误的是( )
选项 |
归类 |
内容 |
A |
清洁能源 |
风能、氢能、太阳能 |
B |
常见合金 |
黄铜、硬铝、不锈钢 |
C |
营养物质 |
淀粉、油脂、维生素 |
D |
复合肥料 |
KNO 3、NH 4H 2PO 4、NH 4NO 3 |
A.AB.BC.CD.D
下列实验设计正确的是( )
A.用活性炭软化硬水
B.用燃烧法区分聚乙烯和聚氯乙烯
C.用托盘天平称取6.45g食盐
D.用NaOH溶液除去CO 2中的HCl
下列对实验现象的描述或实验操作正确的是( )
A.红磷在空气中燃烧,产生大量白雾
B.点燃或加热可燃性气体前,检验其纯度
C.10.0mL酒精与10.0mL蒸馏水混合,溶液的体积为20.0mL
D.用高锰酸钾制取O 2后,应先熄灭酒精灯再从水中取出导气管
自来水消毒过程中常发生下列转化:
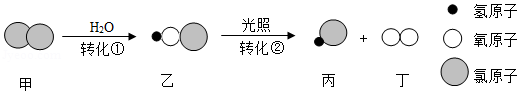
下列说法正确的是( )
A.转化过程中有两种氧化物
B.转化①是化合反应
C.转化②中丙和丁的分子个数之比为1:1
D.转化①、②中氯元素的化合价都发生变化
下列指定反应的化学方程式正确的是( )
A.铝的自我保护:2Al+3O 2═2Al 2O 3
B.用双氧水制氧气:H 2O 2  H 2↑+O 2↑
H 2↑+O 2↑
C.配制波尔多液:CaO+H 2O+CuSO 4=CaSO 4+Cu(OH) 2↓
D.小苏打治疗胃酸多:Na 2CO 3+2HCI═2NaCI+CO 2↑+H 2O
物质性质决定用途.下列说法错误的是( )
A.氮气化学性质稳定,可用于食品保护气
具有碱性,可用于改良酸性土壤
C.食醋具有酸性,可用于除去水壶中的水垢
D.甲醛能使蛋白质变性,可用于食用水产品防腐
下列实验操作中(括号内为杂质)不能达到实验目的是( )
选项 |
物质 |
目的 |
主要实验操作 |
A |
蔗糖、蛋白质溶液 |
鉴别 |
加入饱 溶液,观察现象 |
B |
固体 |
除杂 |
加入适量稀盐酸,蒸发 |
C |
和NaCl的混合物 | 分离 |
溶解、过滤、洗涤、烘干、蒸发 |
D |
空气中NaOH变质程度 |
检验 |
加入足量 溶液,过滤,加酚酞,观察现象 |
A.AB.BC.CD.D
下列说法正确的是( )
A.同种分子构成的物质是纯净物,纯净物一定由同种分子构成
B.某物质燃烧生成CO 2和H 2O,该物质中一定含有C、H、O元素
C.置换反应生成单质和化合物,生成单质和化合物的反应一定是置换反应
D.某化肥与熟石灰研磨,无刺激性气味,该化肥一定不是铵态氮肥
下列各组溶液,不用其它试剂就不能鉴别出来的是( )
A.NaOH、NaCl、稀HNO 3、FeCl 3
B.BaCl 2、MgSO 4、KNO 3、NaOH
C.CuCl 2、稀HCl、NaNO 3、AgNO 3
D.稀HCl、稀H 2SO 4、Na 2CO 3、Ba(NO 3) 2
用化学符号表示:
(1)五氧化二磷 ; (2)地壳中含量最多的元素 ;
(3)最简单的有机物 ; (4)人体缺少 元素会骨质疏松.
选择下列适当的物质填空(选填序号):
A、食盐 B、烧碱 C、硝酸铵 D、武德合金
E、明矾 F、氧气 G、金刚石 H、亚硝酸钠
(1)自然界硬度最大的是 ; (2)可作保险丝的是 ;
(3)生活中作调味品的是 ; (4)溶于水降温的是 ;
(5)可用作医疗急救的是 ; (6)常作净水剂的是 。
常温下进行如图所示实验。
(1)A中固体逐渐减少,发生 (选填“物理”或“化学”)变化。
(2)C中有气泡,溶液颜色 。

观察下列实验,回答问题:
(1)采用冰水浴的原因是 。
(2)写出此实验中反应的化学方程式(其中H 2O 2与生成单质的化学计量数之比为3:2) 。

请结合图1回答问题:
(1)仪器名称:① ,② 。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置 (选填序号)和D组合,反应的化学方程式为 ,二氧化锰的作用是 。
(3)实验室可用装置B或C制H 2,C装置相对于B的优点有 。用E装置收集H 2,气体应从 (选填"a"或"b")端通入。
(4)有同学将实验室制得的CO 2通入澄清石灰水,石灰水未变浑浊,于是作如图2探究:
①实验室制CO 2反应的化学方程式 。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是 。
③装置G的作用是 。

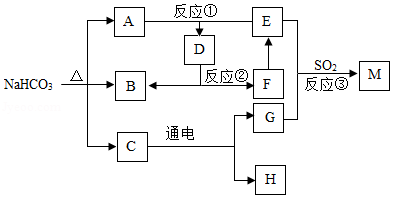
如图为某些物质间的转化关系。E为常见的碱,F常作食品干燥剂,M为石膏的主要成分。部分反应物和生成物已略去。
(1)化学式:C ,F 。
(2)反应①、③的化学方程式:① ,③ 。
(3)能体现明代《天工开物》中"煤饼烧石成灰"的反应是 (选填反应序号)。
(4)工业上可用B和H合成乙醇(C 2H 6O),反应中B和H的质量比为 。
铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
1、上述制品不涉及到的材料是 (选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
2、如图1为出土文物古代青铜铸件"马踏飞燕".该文物能保存至今的原因可能是 (选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
1、我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式: ,2CuO+C  2Cu+CO 2↑.
2Cu+CO 2↑.
2、铁、铜矿石有赤铁矿(Fe 2O 3)、磁铁矿(Fe 3O 4)、黄铁矿(FeS 2)、黄铜矿(CuFeS 2)等.CuFeS 2为二硫化亚铁铜,其中S元素的化合价为 .
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为 .炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;② .
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS 2+17O 2+2H 2SO 4  4CuSO 4+2Fe 2(SO 4) 3+2H 2O.
4CuSO 4+2Fe 2(SO 4) 3+2H 2O.
向上述反应后的溶液中加入Fe粉,得到FeSO 4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe 2(SO 4) 3=3FeSO 4, .
②FeSO 4溶液经蒸发浓缩、 、过滤等操作得到FeSO 4•7H 2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe 2O 3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO 4、Fe 2(SO 4) 3溶液.向溶液中加入过量NaOH溶液得到Cu(OH) 2、Fe(OH) 3固体.
1、证明NaOH溶液过量的方法:静置,向上层清液中滴加 溶液,无现象.
2、用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH) 2分解为CuO;在500℃时,Fe(OH) 3分解为Fe 2O 3.
②在1400℃时,CuO分解为Cu 2O和O 2,Fe 2O 3分解为复杂的铁的氧化物和O 2.
(1)装配好实验装置后,先要 .
(2)停止加热后仍需继续通N 2,可防止倒吸和 .
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
温度/℃ |
室温 |
100 |
550 |
1400 |
B装置/g |
200.00 |
201.80 |
205.04 |
205.04 |
C中铜网/g |
100.00 |
100.00 |
100.00 |
101.28 |
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%= ;ω(Fe)%= .
②复杂的铁的氧化物化学式为 .





 粤公网安备 44130202000953号
粤公网安备 44130202000953号