2017年江苏省南京市中考化学试卷
我国科技创新成果卓越,下列成果中获得诺贝尔奖的是( )
| A. |
侯德榜发明联合制碱法 |
| B. |
屠呦呦发现抗疟新药青蒿素 |
| C. |
闵恩泽研发石油炼制催化剂 |
| D. |
张青莲主持测定了几种元素相对原子质量的新值 |
下列行为会增加空气中PM 2.5的是( )
| A. |
治理工地扬尘 |
B. |
露天焚烧垃圾 |
| C. |
使用公共自行车 |
D. |
禁止焚烧秸杆 |
下列关于干冰升华过程的说法正确的是( )
| A. |
二氧化碳分子的体积变大 |
B. |
二氧化碳分子的质量变小 |
| C. |
二氧化碳分子的种类改变 |
D. |
二氧化碳分子间的间隔变大 |
实验室制取某些气体的装置如图。下列说法正确的是( )

| A. |
装置①和⑤组合可以用来制取氧气 |
| B. |
装置②和③组合可以用来制取氢气 |
| C. |
装置②和④组合可以用来制取二氧化碳 |
| D. |
装置②可以较好地控制反应速率 |
下列叙述不正确的是( )
| A. |
用蒸馏的方法,可以得到净化程度较高的水 |
| B. |
用食醋浸泡鸡蛋的方法,可以制得无壳鸡蛋 |
| C. |
用灼烧闻气味的方法,可以区分棉制品和羊毛制品 |
| D. |
用喷水的方法,可以扑灭所有物质燃烧引起的火灾 |
下列各组离子在水中能大量共存的是( )
| A. |
Cu 2+、Na +、Cl ﹣、OH ﹣ |
B. |
H +、K +、NO 3 ﹣、SO 4 2 ﹣ |
| C. |
Na +、NH 4 +、NO 3 ﹣、OH ﹣ |
D. |
Ag +、Ba 2+、NO 3 ﹣、Cl ﹣ |
除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )
| A. |
FeCl 2溶液(CuCl 2)﹣﹣加入过量的铁粉,过滤 |
| B. |
KCl固体(KClO 3)﹣﹣加入少量的二氧化锰,并加热 |
| C. |
CO气体(CO 2)﹣﹣通过足量的氢氧化钠溶液,并干燥 |
| D. |
NaCl溶液(MgCl 2)﹣﹣加入过量的氢氧化钠溶液,过滤,滤液中加稀盐酸至中性 |
按如图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质生成,无水CuSO 4变蓝,澄清石灰水变浑浊,则X不可能是( )

| A. |
氢气和水蒸气 |
B. |
氢气和二氧化碳 |
| C. |
一氧化碳和氢气 |
D. |
一氧化碳和水蒸气 |
2017年5月,我国首次海域可燃冰试采成功,可燃冰外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等物质。
(1)可燃冰属于 (填"纯净物"或"混合物")。
(2)化学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化属于 (填"物理变化"或"化学变化")。
(3)甲烷(CH 4)可用作燃料,其充分燃烧的化学方程式为 。
(4)常温常压时,由甲烷和另两种气体组成的混合物中,碳元素的质量分数为80%,则另两种气体可能是 。
| A. |
H 2和CO |
B. |
H 2和C 2H 2 |
| C. |
C 2H 2和C 2H 4 |
D. |
CO和C 2H 4 |
溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是 。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水的体积为 mL (水的密度近似看作1g/cm 3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t 1℃时,甲物质的溶解度是 。t 2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填"甲"或"乙")物质的饱和溶液。

(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是 。
选项 |
x |
y |
A |
水 |
氧化钙 |
B |
水 |
硝酸铵 |
C |
浓硫酸 |
水 |
D |
稀盐酸 |
镁 |
核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题。
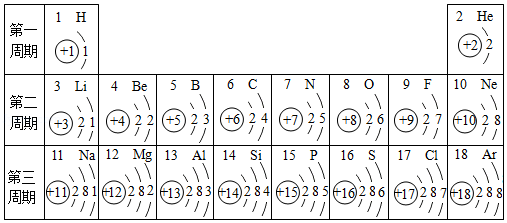
(1)2017年5月9日,中国科学院等单位联合发布了115号元素的中文名为"镆"。此元素原子的核电荷数为 ,核外电子数为 。
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是 。
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化学式各一个,并标出所写化学式中氮元素的化合价:单质 、氧化物 、酸 、碱 、盐 。
(4)以钠和氯为例,简述结构与性质的关系。 。
(5)国产C919大型客机上使用了大量的铝合金。工业上用电解氧化铝(Al 2O 3)得到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(写出计算过程)
空气中氧气含量测定的经典赏析。
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图)。

(1)写出汞与氧气反应的化学方程式 。
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应。②汞为液态,在汞槽中起到液封的作用,并能直接用来测见反应器内空间体积的变化。
③生成的氧化汞分解又能得到汞和氧气,把得到的氧气加到剩下的 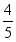 体积的气体中,结果所得气体跟空气的性质完全一样。
体积的气体中,结果所得气体跟空气的性质完全一样。
根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据。
④ 。 ⑤ 。
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积 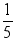 的结论。请根据现在的认识,对此结论予以补充。 。
的结论。请根据现在的认识,对此结论予以补充。 。
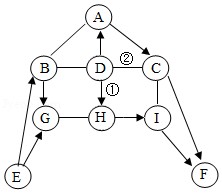
如图中A﹣I表示初中化学常见的物质,且分别是由一种或两种元素组成:其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;H在B、F、G存在的情况下可以生成铜绿[铜绿主要成分为Cu 2(OH) 2CO 3].图中"﹣﹣"表示两端的物质间能发生化学反应:"→"表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出化学式:F ,H 。
(2)实验室常用E制取B,写出该反应的化学方程式 。
(3)反应①和②的基本反应类型相同,该基本反应类型是 。
(4)写出A→C反应的化学方程式 。
兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关探究。
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 |
蒸馏水 |
碳酸氢钠溶液 |
碳酸钠溶液 |
氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 |
蓝紫色 |
蓝色 |
绿色 |
黄色 |
查阅资料:
pH |
7.5~9 |
10~11.9 |
12~14 |
紫甘蓝汁液显示的颜色 |
蓝色 |
绿色 |
黄色 |
【得出结论1】三种溶液的碱性由强到弱的顺序为 。
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由 色变为 色。向其中加入稀盐酸,该反应的化学方程式为 。
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1所示。a点表示的意义是: 。
【得出结论2】从微观角度分析,该反应的实质是 。
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图2、图3所示。
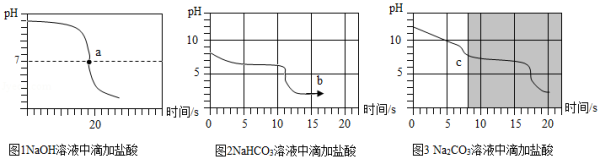
【交流与反思】b点的溶质为 (写化学式),将图2和图3的阴影部分进行叠加,发现两者基本重合,c点的溶质 (写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式表示: 、 。
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进行的过程。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号