2016年江苏省泰州市中考化学试卷
下列化学用语书写正确的是( )
| A. |
铝元素 AL |
B. |
干冰 H 2O |
C. |
氢氧根离子 OH ﹣ |
D. |
氯化银 AgCl 2 |
下列实验操作不符合规范要求的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
下列事实,不适合用"微粒间有空隙"的性质来解释的是( )
| A. |
一定体积的气体加压后体积变小 |
| B. |
一定量的水结冰后体积变大 |
| C. |
室外的电线在冬天变短夏天变长 |
| D. |
1L大豆与1L黄沙混合总体积小于2L |
下列关于燃烧与灭火的说法,正确的是( )
| A. |
放在空气的木桌椅没有燃烧,是因为木桌椅不是可燃物 |
| B. |
防止森林大火蔓延,开挖隔离带,是为了将可燃物与火隔离 |
| C. |
油锅着火,用锅盖盖上,是为了降低可燃物的温度 |
| D. |
住房失火,消防队员用水扑灭,是为了降低可燃物的着火点 |
下列有关实验的描述,正确的是( )
| A. |
镁在空气中燃烧,火星四射,生存黑色固体 |
| B. |
配制一定质量分数的氯化钠溶液,一般步骤为:计算、称量、溶解、转移 |
| C. |
将固体氢氧化钠溶于水中,溶液的温度显著降低 |
| D. |
将棉花点燃,闻到一股烧焦羽毛的气味 |
图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )

| A. |
t 1℃时,三种固体物质的溶解度关系为乙>甲=丙 |
| B. |
t 2℃100g甲物质饱和溶液中含有60g甲 |
| C. |
将丙物质饱和溶液变为不饱和溶液,可采用升温的方法 |
| D. |
t 2℃时,分别用100g水配制甲、乙的饱和溶液,再降温到t 1℃,析出无水晶体的质量:甲>乙 |
下列说法正确的是( )
| A. |
分子可以直接构成物质,则溶质都以分子形式分散到溶剂中形成溶液 |
| B. |
中和反应生成盐和水,则生成盐和水的反应都是中和反应 |
| C. |
铵盐能与碱反应生成氨气,则硫酸铵不能与熟石灰混合施用 |
| D. |
一氧化碳、二氧化碳组成元素相同,则一氧化碳、二氧化碳化学性质相同 |
下列除杂(括号内为杂质)设计,所选试剂和操作方法均正确的是( )
选项 |
物质 |
所选试剂 |
操作方法 |
A |
HCl气体(H 2O) |
固体氢氧化钠 |
通过装有试剂的干燥管,收集 |
B |
CaCl 2溶液(HCl) |
碳酸钙粉末 |
加过量试剂,充分反应,过滤 |
C |
KNO 3溶液(CuSO 4) |
Ba(OH) 2溶液 |
加过量试剂,充分反应,过滤 |
D |
CaCO 3固体(CaCl 2) |
水 |
加足量试剂,溶解、过滤、蒸发结晶 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
海水是一种重要的资源,利用海水可制取镁等物质.有人设计如图实验流程:
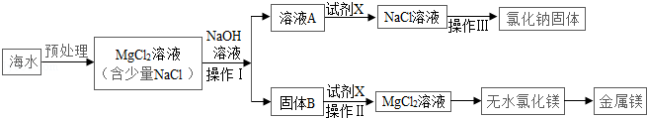
下列说法错误的是( )
| A. |
固体B是Mg(OH) 2,试剂X为盐酸 |
| B. |
操作Ⅰ和操作Ⅲ的操作方式完全相同 |
| C. |
加入NaOH溶液应过量,其目的是使MgCl 2完全反应 |
| D. |
处理等量海水,若将NaOH溶液换成石灰乳,既能节约成本,又能提高镁的产量 |
生活离不开化学.
(1)地球上各种生物活动所需要的能量主要来自于 能,绿色植物通过 作用将CO 2和H 2O转化为葡萄糖和氧气.植物秸秆还可用于发酵制取沼气,沼气主要成分为甲烷,甲烷的化学式为 .
(2)香烟燃烧产生的烟气中含有尼古丁(化学式为C 10H 14N 2),焦油和CO等有害物质,其中尼古丁属于 (填"有机物"、"无机物"),尼古丁中C、H、N三种元素的原子个数最简比为 .
(3)草木灰的浸出液中含有碳酸钾,向少量浸出液中滴入2滴紫色石蕊试液,溶液呈蓝色,说明草木灰的浸出液显 性(填"酸"或"碱"或"中");碳酸钾中阳离子的符号是 .
(4)快热食品包装袋内部有一夹层,夹层内分开放置生石灰(CaO)、水,使用时将两种物质接触发生化学反应而放出热量,化学方程式可表示为 .利用这一反应,在保存食品时,生石灰可作为 (填"干燥剂"、"补钙剂"、"着色剂").
同学们利用如图所示装置进行气体的制备实验(A~F为装置编号)。

(1)写出图D装置中甲仪器的名称 。
(2)用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为 ,其中二氧化锰起 作用;收集氧气可以选择 (填装置编号)。
(3)实验室制取CO2通常选择下列药品中的 (填药品序号)。
a、稀盐酸 b.熟石灰 c.块状石灰石 d.稀硫酸
通常检验CO2气体的反应可用化学方程式表示为 。
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是 (填装置编号,下同)。实验室制取氢气应选择的发生和收集装置的组合可以使 。
(5)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是 (填序号)。
a.将烧杯换成水槽 b.导管深入水中位置过深,气体无法逸出
c.将水换成冰水 d.先用手捂住试管壁,再将导管另一端插入水中。
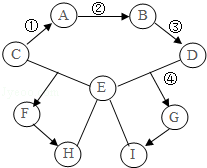
A~I为初中化学常见物质,相互转化关系如图所示,“→”表示转化关系,“﹣”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略)。
其中,A、C、F、H含相同金属元素且所属物质类别不同,H、I类别相同;A、B为金属单质,B为紫红色;C、D为氧化物,C为红棕色固体;G溶液呈蓝色,E的浓溶液常用作某些气体的干燥剂。请回答下列问题:
(1)C的化学式 ;E的化学式 。
(2)F溶液的颜色 ;I所属物质类别是 。
(3)写出化学反应方程式:反应① ;反应④ 。
(4)在①②③④四个反应中,未涉及到的基本反应类型为 反应。
"84"消毒液在日常生活中使用广泛,具有漂白、杀菌、消毒功效。某化学兴趣小组对一瓶敞口久置的"84"消毒液成分产生兴趣,在老师的指导下,展开探究。
【提出问题】该敞口久置的消毒液中溶质有哪些?
【查阅资料】"84"消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO 2反应(2NaClO+CO 2+H 2O═2HClO+Na 2CO 3)。NaClO溶液、HClO都具有漂泊、杀菌、消毒功效。HClO不稳定,受热或光照会发生分解。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有 。可能还有NaClO、Na 2CO 3、HClO中的一种或多种。
【实验过程】Ⅰ:向装入有色布条的试管中加入适量该消毒液试样,布条长时间不褪色。
Ⅱ:另取适量该消毒液试样于试管中,加入足量氯化钙溶液,静置,观察到的现象为 。
【得出结论】实验过程Ⅰ中有色布条不褪色,说明该消毒液试样中的溶质不含 。实验过程Ⅱ中反应的化学方程式为 。综上所述,该消毒液试样中的溶质为 。
【交流反思】生活中,"84"消毒液贮藏时应注意 ;一般不要"84"消毒液对蔬菜、水果进行消毒,其原因可能是 。
【拓展延伸】(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为
(2)次氯酸钠与盐酸反应可生成有毒的氯气,日常生活中"84"消毒液不能与洁厕灵(主要成分为盐酸)混合使用。
 加热烧杯中液体
加热烧杯中液体 放置洗净的试管
放置洗净的试管 锌粒放入试管
锌粒放入试管 嗅闻气体气味
嗅闻气体气味
 粤公网安备 44130202000953号
粤公网安备 44130202000953号