2016年湖北省宜昌市中考化学试卷
2016年6月5日世界环境日中国主题是“改善环境质量,推动绿色发展”。下列做法符合这一主题的是( )

A.鼓励燃煤发电,确保电力供应
B.提倡公交出行,减少尾气排放
C.就地焚烧秸秆,增加田间肥料
D.燃放烟花爆竹,增强节日气氛
下列实验现象描述正确的是( )
A.铁丝伸入盛氧气的集气瓶中剧烈燃烧
B.红磷在空气中燃烧产生大量白雾
C.硫燃烧时生成有刺激性气味的气体
D.氢氧化钠溶于水时溶液温度降低
强化安全意识,提升安全素养。下列采取的安全措施错误的是( )
A.在点燃氢气前先检验其纯度
B.在火灾逃生时用湿毛巾捂住口鼻
C.在加油站张贴严禁烟火标志
D.在天然气燃气灶下方安装报警器
溴元素的原子结构示意图及其在周期表中的信息如图所示。下列说法错误的是( )

A.n=5B.该元素为非金属元素
C.形成的离子是Br﹣D.原子序数为35
某纯净物M燃烧的化学方程式为:M+3O2 2CO2+2H2O,则M的化学式是( )
2CO2+2H2O,则M的化学式是( )
A.C2H2B.C2H4C.C2H6D.C2H4O
“部分酸、碱和盐的溶解性表(室温)”是学习化学的重要工具,如表是截取溶解性表中的一部分,有关①处物质的说法不正确的是( )
阴离子 阳离子 |
OH﹣ |
Cl﹣ |
… |
… |
… |
Fe2+ |
不 |
① |
… |
… |
… |
A.①处物质的化学式是FeCl2
B.①处物质的名称是氯化铁
C.①处物质可溶于水
D.①处物质类别属于盐
除去下列物质中的少量杂质,实验方案不能达到除杂目的是( )
物质(括号内为杂质) |
实验方案 |
|
A |
氮气(氧气) |
通过足量灼热铜网 |
B |
氧化铜(木炭粉) |
在空气中充分灼烧 |
C |
铜粉(铁粉) |
加入足量稀盐酸,过滤,洗涤,干燥 |
D |
硫酸锌溶液(硫酸) |
加入足量氧化铁粉末,过滤 |
A.AB.BC.CD.D
能验证Zn、Cu、Ag三种金属活动性顺序的一组试剂是( )
A.Zn、Ag、CuSO4溶液
B.Zn、Cu、Ag、H2SO4溶液
C.Cu、Ag、ZnSO4溶液
D.Ag、ZnSO4溶液、CuSO4溶液
如图中“﹣”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质,部分反应物、生成物及反应条件未标出.则不可能出现的情况是( )

A.甲是H2、乙是O2
B.甲是HNO3,丙是NaNO3
C.乙是CO,丙是CO2
D.乙是Cu(OH)2、丙是CuSO4
下列实验能用如图表示的是( )

A.向硫酸铜溶液中加入铁粉
B.向过氧化氢溶液中加入二氧化锰
C.向一杯接近饱和的石灰水中加入氧化钙
D.向不饱和的硝酸钾溶液中加入硝酸钾
下列归纳总结完全正确的一组是( )
A.化学之最 |
B.化学与生活 |
①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 ③天然存在的最硬的物质是金刚石 |
①衣服上的油污:可用汽油除去 ②水壶中的水垢:可加食盐水浸泡除去 ③冰箱中的异味:可放活性炭吸附 |
C.物质保存方法及解释 |
D.化学与工农业 |
①浓盐酸密封保存:防止挥发 ②白磷在冷水中保存:隔绝空气 ③氢氧化钠密封保存:防止潮解、变质 |
①用焦炭和铁矿石炼铁 ②用石油产品生产合成纤维 ③施用过量化肥,农药增加粮食产量 |
A.AB.BC.CD.D
学习生活中的化学,解释生活中的现象,化学就在我们身边。
(1)如图是常见的电源插头,在标示的部分中,属于有机合成材料的是 。
(2)铜能制成插头和导线,是利用了金属铜的 性和 性。
(3)厕所用清洁剂(含盐酸)不慎洒到大理石地面上,会发出嘶嘶声。用化学方程式表示原因: 。
(4)我国药学家屠呦呦因研制新型抗疟药膏素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。东晋名医葛洪《肘后备急方》中就有青蒿素抗疟的记载:“青蒿一握,以水二升渍,绞取汁,尽服之”。这里的“水”作 。上述水煎青蒿治疗疟疾,药性很不稳定,效果很差,屠呦呦改用乙醇提取,控温60℃,药性显著提高,说明青蒿素具有的性质是(答一条): 。

甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题:
(1)t3℃时,甲物质的溶解度是 .
(2)t2℃,把甲、乙、丙三种物质的饱和溶液降温到t1℃,溶质质量分数不变的是 .
(3)t2℃时,把20g乙物质加到50g水中,充分搅拌后所得溶液的质量是 g;若要让乙物质从它的饱和溶液中全部结晶析出,应采取的方法是 .

“魔力蜡烛”可以增加生日宴会气氛.制造蜡烛时,在烛心中掺入镁粉(镁粉在430℃时能自燃).每次吹灭蜡烛时,余烬会引燃烛心中的镁粉,产生火花,又重新点燃蜡烛.
(1)镁粉燃烧的化学方程式为 .
(2)“魔力蜡烛”能“死灰复燃”,说明燃烧的条件之一是 .
如图是实验室常用气体制备装置,据图回答问题:

(1)用A装置制取氧气的化学方程式是 。选择D装置收集氧气是因为 。将带火星的木炭深入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能 ,该反应的化学方程式为 。
(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固) CaCl2(固)+2H2O+2NH3↑,要制取并收集干燥的氨气,所选装置正确的连接顺序是 → → (填字母代号)。
CaCl2(固)+2H2O+2NH3↑,要制取并收集干燥的氨气,所选装置正确的连接顺序是 → → (填字母代号)。
(3)为探究氨气的性质,按如图装置进行实验。观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成。

【查阅资料】Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O。
【提出问题】得到的红色物质是什么?
【猜想】①是Cu;②是Cu2O;③是 。
若猜想①成立,玻璃管中发生反应的化学方程式为 ,说明NH3具有 性。
【设计实验】请你设计一个简单的实验来验证红色物质中是否存在Cu2O: 。
氢气是理想的清洁高能燃料,以水为原料生产氢气的方法有多种。
方法Ⅰ:电解水法。写出电解水的化学方程式 。
方法Ⅱ:光解水法。我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“〇”表示氢原子,“●”表示氧原子,“▁”表示催化剂)。
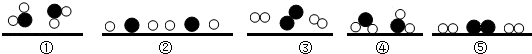
则水分解微观过程的正确顺序是 (填数字序号)。上述过程中,不能再分的粒子是 。
控制变量,设计对比实验是实验探究的重要方法.
实验编号 |
一、探究人体呼出气体中二氧化碳含量比空气中的高 |
二、探究影响品红扩散快慢的因素 |
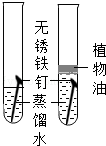
三、铁钉锈蚀条件的探究 |
实验设计 |
|
|
|
实验分析 |
本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制 相同 |
发现两杯水都变红,且整杯热水变红时间比冷水要短.由此说明:分子在不断运动;影响分子运动快慢的因素有 . |
一周后,左边试管中铁钉生锈,右边试管中铁钉无明显变化.上述实验 (填“能”或“不能”)得出铁钉生锈的条件. |
工业烟气脱硫就是将烟气中含有的二氧化硫除去。一种采用“双碱法”脱硫的工业流程示意图如图:
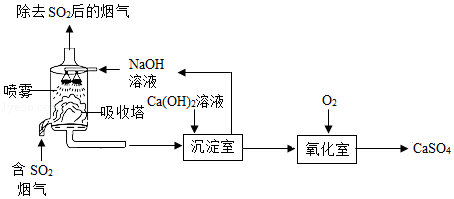
(1)吸收塔中,用NaOH溶液吸收SO2,生成 和H2O.NaOH溶液喷成雾状能充分吸收SO2的原因是 。
(2)沉淀室中,发生反应的化学方程式为 。
(3)氧化室中,化学反应的基本类型是 反应。
(4)上述流程中,可以循环利用的物质是 ,有利于节约成本。
设计方案是实验探究的保证,感悟方法是探究的根本目的。某合作学习小组开展了如下探究。
实验一:检验氢氧化钠溶液中是否含有氢氧化钙。
【分析】从组成上看,氢氧化钙和氢氧化钠都属于碱,它们在水溶液中都能解离出相同的 (填符号),所以具有相似的化学性质。但由于解离出的Na+和Ca2+不同,所以性质也有不同。设计实验时可加入能解离出CO32﹣的试剂利用CO32﹣与Ca2+结合产生白色沉淀这一特殊现象予以检验。
【设计方案并实验】
实验操作 |
现象 |
结论 |
|
方案一 |
取少量待测溶液于试管中,通入CO2 |
出现白色沉淀 |
氢氧化钠溶液中含有氢氧化钙 |
方案二 |
取少量待测溶液于试管中,滴加 溶液 |
出现白色沉淀 |
写出上述方案中出现白色沉淀的一个化学方程式 。
【方法感悟】在检验物质时,要分析物质的组成和 。据此选择加入恰当的试剂,最后根据不同现象得出结论。
【实验探究】
实验二:有一种白色固体,可能含有氯化钠、氢氧化钠、碳酸钠、硫酸钠和硝酸钡中的一种或几种,为探究其组成,某合作学习小组设计方案并进行了如图实验:

(1)上述实验中,过滤操作用到的玻璃仪器有:烧杯、玻璃棒和 。
(2)小晶同学通过上述实验推知:白色固体样品中一定不含有 。
(3)为确定白色固体样品中可能存在的物质,小燕对沉淀C进行实验。
实验操作 |
现象 |
结论 |
取少量沉淀C于试管中,加入过量 。 |
有气泡产生,沉淀全部消失。 |
白色固体样品中一定含有 。 |
(4)小虎同学认为白色固体中还有物质不能确认其是否存在。其理由是(用化学方程式表示): 。如要确认,只需将上述实验方案中所加的一种试剂改为 即可。
【方法感悟】若其他物质的存在对所检验的物质有干扰时,可先将干扰物质转化,再选择加入恰当的试剂,最后根据不同现象得出结论。
钙是人体必须的常量元素,葡萄糖酸钙(C12H22O14Ca)是一种常用的补钙剂.
(1)葡萄糖酸钙中碳、氢元素的质量比为 .
(2)葡萄糖酸钙中钙元素的质量分数比为 (保留一位小数).
 B.稀释浓硫酸
B.稀释浓硫酸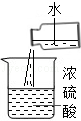
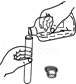 D.读取液体体积
D.读取液体体积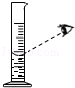


 粤公网安备 44130202000953号
粤公网安备 44130202000953号