安徽省马鞍山市高一第二学期期末测试化学试卷
光导纤维被认为是20世纪最伟大的发明之一。光导纤维的主要成分是
| A.Si | B.SiO2 | C.Na2SiO3 | D.SiCl4 |
下列关于SO2的说法中,不正确的是
| A.SO2是硫及某些含硫化合物在空气中燃烧的产物 |
| B.SO2具有漂白性,可以使品红溶液褪色 |
| C.SO2与水反应生成H2SO4 |
| D.SO2既有氧化性又有还原性 |
实现下列变化,一定要加入氧化剂的是
| A.HCl→Cl2 | B.Na2SO3→SO2 | C.HCl→H2 | D.HNO3→NO |
现有两瓶溶液,新制饱和氯水和亚硫酸,下列方法或试剂(必要时可加热)能用于鉴别它们的是
①观察颜色 ②石蕊试液 ③品红溶液
| A.① ② ③ | B.只有① ③ | C.只有② ③ | D.只有① ② |
检验某未知溶液中是否含有SO42-的下列操作中,最合理的是
| A.加入盐酸酸化的硝酸钡溶液 | B.先加硝酸酸化,再加硝酸钡溶液 |
| C.加入盐酸酸化的氯化钡溶液 | D.先加盐酸酸化,再加氯化钡溶液 |
能证明硅酸的酸性弱于碳酸酸性的实验事实是
| A.CO2溶于水并能形成碳酸,SiO2难溶于水 |
| B.CO2通入可溶性硅酸盐中析出硅酸沉淀 |
| C.高温下SiO2与C反应生成CO |
| D.氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀 |
下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.放热反应在常温下一定很容易发生 |
| C.反应是放热还是吸热,可根据反应物和生成物所具有的总能量的相对大小判断 |
| D.吸热反应在常温下一定不能发生 |
下列表达方式错误的是
| A.氯化氢分子的电子式: | B.S2-的结构示意图是: |
C.O—18原子的符号: |
D.CO2分子的结构式:O=C=O |
下列物质中,既含有离子键又含有非极性键的是
| A.CO2 | B.MgCl2 | C.KOH | D.Na2O2 |
不同金属的冶炼,其冶炼方法也可能不同,主要原因是在自然界中金属的
| A.含量不同 | B.分布不同 | C.活动性不同 | D.存在形式不同 |
某些建筑材料含有放射性元素氡( ),会对人体产生一定危害。该原子里中子数和质子数之差是
),会对人体产生一定危害。该原子里中子数和质子数之差是
| A.50 | B.86 | C. 136 | D.222 |
某碱性溶液中,可以大量共存的离子组是
| A.K+、Na+、HCO3-、NO3- | B.H+、Mg2+、SO42-、NO3- |
| C.Na+、SO42-、Cl-、ClO- | D.Ag+、K+、NO3-、Na+ |
在碘化钾溶液中加入适量氯水充分反应,并将反应后的溶液分成四份于试管中,编号为I、II、Ⅲ、Ⅳ,分别加入汽油、CCl4、酒精、NaCl溶液,振荡后静置,下列现象描述正确的是
| A.I中溶液分层.上层无色 | B.Ⅱ中溶液分层,下层紫红色 |
| C.Ⅲ中溶液分层,下层呈棕色 | D.Ⅳ中溶液不分层,溶液由棕色变成黄绿色 |
一定条件下,反应N2+3H2 2NH3,在2L密闭容器中进行,5min内氨物质的量增加了0.1mol,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨物质的量增加了0.1mol,则反应速率为
| A.v(H2)=0.03mol/(L·min) | B.v(N2)=0.02mol/(L·min) |
| C.v(NH3)=0.1mol/(L·min) | D.v(NH3)=0.01mol/(L·min) |
右图是可逆反应X2 + 3Y2 2Z2在反应过程中的反应速率(V)与时(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(V)与时(t)的关系曲线,下列叙述正确的是
| A.t1时,只有正方向反应 |
| B.t2时,反应到达限度(或平衡) |
| C.t2- t3,反应不再发生 |
| D.t2- t3,各物质的浓度相等 |
下列物质能通过化合反应直接制得的是
①FeCl2 ②H2 SO4 ③NH4Cl ④NO
| A.只有①②③ | B.只有②③④ | C.只有①③④ | D.全部 |
某元素原子的质量数为A,它的阳离子Xn+核外有x个电子,w克这种元素的原子核内中子数为
A. |
B. |
C. |
D. |
将充有m mL NO和n mL NO2的量筒倒立于水槽中,然后通入m mL O2,若m<n,则充分
反应后,量筒内气体体积的毫升数为
A.3(m-n) B. C.m+ D.
下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 一 |
① |
|
|
|||||
| 二 |
|
|
|
② |
③ |
④ |
⑤ |
|
| 三 |
⑥ |
|
⑦ |
|
|
⑧ |
⑨ |
⑩ |
(1) 在这些元素中,化学性质最不活泼的是: (填元素符号)。
(2) 元素②和③非金属性较弱的是___________(填元素符号),画出元素③原子结构示意图_______________________。
(3) ④和⑧气态氢化物的稳定性较强的是_____________(填化学式)。
(4) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是___________,碱性最强的化合物的电子式是___________________。
(5)用电子式表示元素①和⑤所形成化合物的形成过程:________________________。
(6)⑤⑥⑦三种元素分别形成的单核离子半径由大到小顺序为________________(填离子符号)。
(7)元素①和④按原子个数比1:1形成的化合物分解的化学方程式_________________。
(8)写出元素⑦和⑨最高价氧化物的水化物之间反应的离子方程式_________________。
(1)如图,若烧瓶是干燥的。当烧瓶口向上时,由A口导入气体,可收集下列中的 (填序号,下同)气体。若烧瓶充满水,可收集下列中的________气体。
①NO ②NH3 ③SO2 ④NO2
(2)若烧瓶中事先已集满一瓶氨气,并将烧瓶口向下放置,由______口导入气体可收集NO气体,其原因是 __________________________________________________。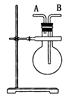
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
| 实验方案 |
实验现象 |
||||
| ①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞。 ②向新制的H2S饱和溶液中滴加新制的氯水 ③钠与滴有酚酞试液的冷水反应 ④镁带与2mol/L的盐酸反应 ⑤铝条与2mol/L的盐酸反应 |
E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的: 。
(2)实验用品:仪器、材料: 略 药品: 略
(3)实验内容:用序号填写下表中的实验方案,并完成相关的离子方程式
| 实验方案 |
实验现象 |
有关离子方程式 |
| |
A |
|
| |
B |
不填 |
| |
C |
不填 |
| |
D |
不填 |
| |
E |
|
(4)实验结论:____________________________________________________。
(5)请用原子结构理论解释上述结论的原因___________________________
实验室常用下图装置制取氨气:请回答下列问题:
(1)写出图中带有编号的仪器名称a___________ b___________。
(2)写出该实验中制取氨气的化学方程式:________________________________。
(3)检验氨气是否收集满的方法是__________________________________。
(4)不用排水法收集氨气的原因是:_________________________。
(5)试管口棉花的作用是:_________________________________。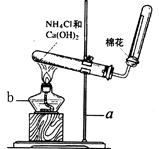
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有_________________________________________;
__________________________________________。
(2)加入硫酸铜溶液后可以加快氢气生成速率的原因是_____________________________。
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是________。
(4)要加快上述实验中氢气生成速率,还可采取的措施有___________________________
____________________________________________________________ (答两种即可)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验:
| 实验 混合溶液 |
A |
B |
C |
D |
E |
F |
| 4 mol/L H2SO4(mL) |
30 |
V1 |
V2 |
V3 |
V4 |
V5 |
| 饱和CuSO4溶液(mL) |
0 |
0.5 |
2.5 |
5 |
V6 |
20 |
| H2O(mL) |
V7 |
V8 |
V9 |
V10 |
10 |
0 |
将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=__________,V6=__________,V9=________。
②反应一段时间后,实验A中的金属呈________色,实验E中的金属呈________色。
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_____________________________________________________________________________________________________________________________。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号