上海市闸北区九年级上学期期中测试化学试卷
下列物质中,前一种物质是氧化物,后一种物质是混合物的是
| A.生石灰、熟石灰 | B.碳酸、二氧化碳 |
| C.水、澄清石灰水 | D.胆矾、空气 |
雾霾是一种大气污染现象,不属于雾霾治理措施的是
| A.植树绿化,美化环境 | B.提倡绿色出行,发展公共交通 |
| C.外出时佩戴反雾霾口罩 | D.减少燃煤发电,增加太阳能发电 |
(34)三氧化二铬(Cr2O3)可用作油漆颜料,Cr2O3中Cr的化合价是
| A.-3 | B.-2 | C.+2 | D.+3 |
下列物质的化学式的读法和写法都正确的是
| A.胆矾CuSO4·5H2O | B.碳酸钠NaCO3 | C.氢氧化铝AlOH3 | D.氧化铁FeO |
调查统计表明,火灾伤亡事故很多是由于缺少自救常识造成的,缺氧窒息是致人死亡的首要原因。相关自救措施不合理的是
| A.在山林中遇火灾时,尽量向逆风方向奔跑,脱离火灾区 |
| B.有烟雾的地方,尽量贴近地面逃离 |
| C.烟雾很大时,用湿毛巾捂住口鼻 |
| D.室内起火,立即打开所有门窗 |
某物质在空气中燃烧后生成二氧化硫和水,该物质
| A.只含硫元素 | B.一定含氧元素 |
| C.一定含硫、氧、氢元素 | D.一定含硫、氢元素,可能含氧元素 |
有关水分子的叙述正确的是
| A.水在固态时分子是静止不动的 |
| B.水结冰后体积变大是水分子的体积增大造成的 |
| C.保持水的化学性质的微粒是水分子 |
| D.水由液态变成气态时水分子质量变小 |
科研人员发现维生素P 能封住病毒的侵占途径。已知维生素P 的化学式为C27H30O16,关于维生素P的叙述中正确的是
| A.维生素P是由27个碳原子、30个氢原子和16个氧原子构成 |
| B.维生素P是一种氧化物 |
| C.维生素P的式量为610 g |
| D.将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O |
氢气在氯气中燃烧的化学方程式是H2+Cl2 2HCl,该反应属于
2HCl,该反应属于
| A.分解反应 | B.化合反应 | C.复分解反应 | D.置换反应 |
关于物质燃烧的现象描述错误的是
| A.磷在空气中燃烧,反应剧烈,产生大量白雾 |
| B.铁丝在氧气中燃烧,火星四射,生成黑色固体 |
| C.镁带在空气中燃烧,发出耀眼的白光,生成白色固体 |
| D.硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体 |
物质的性质决定用途,下列物质的用途主要由其化学性质决定的是
| A.用活性炭吸附有色物质 | B.用金刚石做钻头 |
| C.用石墨做铅笔芯 | D.用焦炭冶炼金属 |
关于水的净化过程描述错误的是
| A.加入明矾使小颗粒凝聚 | B.通入氯气杀菌消毒 |
| C.通过沙滤装置除去可溶性杂质 | D.通过活性炭吸附部分有害物质 |
有关实验操作正确的是
| A.加热蒸发皿时垫上石棉网 | B.将氢氧化钠固体放入烧杯中称量 |
| C.在量筒中溶解氯化钠固体 | D.将pH试纸浸入待测液中测定pH |
“绿色化学”是21世纪化学发展的主导方向,“绿色化学”要求从根本上消除污染,它包括“原料的绿色化”、“化学反应绿色化”、“产物绿色化”等内容。其中(化学反应绿色化)要求原料物质中所有的原子完全被利用且全部转化入期望的产品中。下列反应中符合“化学反应绿色化”的是
| A.用氯酸钾和二氧化锰制取氧气 | B.工业上制取氧气 |
| C.2C2H4+ O2 → 2C2H40 | D.天然气燃烧生成二氧化碳和水 |
SiO2是制造光导纤维的主要原料,下列关于SiO2的说法正确的是
| A.SiO2的摩尔质量是60 |
| B.1mol SiO2中含有1molO2 |
| C.1.5mol SiO2中含有1.806×1024个氧原子 |
| D.1mol SiO2的质量是60g/mol |
将一定量的乙醇(C2H5OH)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
| 物质 |
乙醇 |
氧气 |
水 |
二氧化碳 |
X |
| 反应前质量/g |
9.2 |
16.0 |
0 |
0 |
0 |
| 反应后质量/g |
0 |
0 |
10.8 |
8.8 |
a |
下列判断正确的是
A.无论如何改变氧气的起始量,均有X生成
B.X一定是该反应的催化剂
C.X不含氢元素
D.表中a的值为6.6
苯(C6H6)是室内装潢污染物之一,它的摩尔质量是 ,0.5 mol 苯的质量是 克,0.5 mol 苯含碳原子的物质的量是 mol,含 个氢原子。苯完全燃烧生成二氧化碳和水,请写出苯完全燃烧时的化学方程式: 。
有一种干燥剂,它的主要成分是生石灰,其化学式为 。将该干燥剂放入水中搅拌,其中主要反应的化学方程式是 ,滴入无色酚酞显 色。反应后,取出少量清夜于试管中,再向这清液中吹气,有关的化学反应方程式为 。
电解水的实验装置如图所示,根据图回答:

(1)电源中A端是电源的 极(填“正”或“负”)。
(2)试管d中气体是 。
(3)若收集到c气体22.4mL,则理论上应收集到d气体大约 mL。
(4)该反应的化学方程式是 ,电解水时发生改变的粒子是 ,电解水时没有变化的粒子是 。
(5)电解水的实验说明:水是由 组成的化合物。
铜是一种常用的金属,纯净的铜颜色为紫红色,它能够和硝酸银溶液发生化学反应,生成硝酸铜和银单质。某同学设计下表所示实验,探究金属铜对过氧化氢溶液分解速率的影响。
| 操作 |
装置 |
现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上。 |
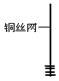 |
 |
| 2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中。 |
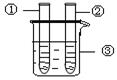 |
约1min后可观察到①和②中都有少量气泡产生 |
| 3、把铜丝插入①中。 |
 |
①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生 |
(1)仪器②中实验的目的是__________________________;
(2)根据上述实验,可以得出的结论是______________________________;
(3)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是___________________。
A.称量实验前铜丝网的质量 B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰 D.将实验后的铜丝网插入AgNO3溶液中。
用下图所示装置制备常见气体。请回答下列问题:

(1)写出图中标号①和②的仪器名称: 、 。
(2)小明用上图B、E装置制取一种常见气体。
①请写出有关反应的化学方程式 。
②检查装置的气密性:先将B装置的导管浸入水中,然后用手握住试管外壁,观察到导管口 (填“有”或“没有”)气泡冒出,表明B装置肯定会漏气。
③如何检验D中的气体已收集满?请写出有关的操作和现象 。
④收集气体时,要等到有连续稳定气泡冒出时才开始收集,而不是一看到气泡冒出就收集气体,其原因是 。
(3)利用上述实验仪器收集气体时,若只能用C装置收集,则该气体必须具备的性质是 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号