广东省中山市高三化学模拟试卷(九)
下列物质与常用危险化学品的类别不对应的是
A. 、 、 ——腐蚀品 ——腐蚀品 |
B. ——易燃液体 ——易燃液体 |
C. ——遇湿易燃物品 ——遇湿易燃物品 |
D. ——氧化剂 ——氧化剂 |
NA为阿伏加罗常数,下列有关说法正确的是
| A.在120g NaHSO4晶体中,含阳离子数为2NA | |
| B.足量的铜与含2molH2SO4的浓硫酸充分反应,可生成NA个SO2分子 | |
| C.500mL 2mol·L-1 Na2CO3溶液中,含NA个CO32- .... |
D.1mol H3O+ 中含有电子数为10NA |
下列说法正确的是
A.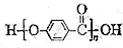 的结构中含有脂基 的结构中含有脂基 |
| B.顺-2-丁烯和反-2-丁烯的加氢产物不同 |
C.1 葡萄糖可水解生成2 葡萄糖可水解生成2 乳酸( 乳酸(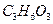 ) ) |
| D.脂肪和蛋白质都是能发生水解反应的高分子化合物 |
用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是
| A.上下移动①中铜丝可控制SO2的量 |
| B.②中选用品红溶液验证SO2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
D.为确认 生成,向①中加水,观察颜色 生成,向①中加水,观察颜色 |
下列液体均处于25℃,有关叙述正确的是
A.无色溶液中:NH 、Ag+、PO 、Ag+、PO 、Cl—能大量共存 、Cl—能大量共存 |
| B.pH= 4.5的番茄汁中c(H+)是pH= 6.5的牛奶中c(H+)的2倍 |
| C.AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同 |
| D.pH= 7的CH3COOH与CH3COONa混合溶液中,c(Na+) = c(CH3COO-) |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e-=4OH- |
| C.每转移0.1 mol电子,消耗1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
J、L、M、R是原子序数依次增大的短周期主族元素,J、M在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;L是地壳中含量排第二位的元素。下列说法正确的是:
| |
J |
|
|
|
| |
|
|
M |
|
| A.J 在周期表的位置是第二周期ⅣA族 |
| B.M元素的氢化物在同主族元素氢化物中最稳定 |
| C.R元素的最高价氧化物对应的水化物的酸性最强 |
| D.L的氧化物易溶于水 |
下列反应的离子方程式正确的是
A.过量SO2通入到Ba(NO3)2溶液中:3SO2+2NO +3 Ba
+3 Ba +2H2O="3" BaSO4↓+2NO+4H
+2H2O="3" BaSO4↓+2NO+4H
B.铝铵矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
C.H2O2溶液中滴加酸性KMnO4溶液: 2 MnO4-+5 H2O2+6H+=2Mn2++5O2↑+8H2O
D少量NaHSO4溶液与足量Ba(OH)2溶液反应离子方程式为:
H++SO2-4+Ba2++OH-=BaSO4↓+H2O
(一)糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_____________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和________ ____(写结构简式或名称)。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:________________________。
(二)茉莉花香气的成分有多种,乙酸苯甲酯( )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
(1)C的结构简式为_______________。
(2)写出反应①的化学方程式:______________ __________ 。
(3)反应③的反应类型为______________ _______________。
(4)反应______ ____(填序号)原子的理论利用率为100%,符合绿色化学的要求。
(16分)氨气是一种重要的基础化工原料,用途广泛。
在微电子工业中,氨水可作刻蚀剂H2O2的清除剂,产物不污染环境。该反应的化学方程式为2NH3+3H2O2= +6H2O
工业中常用以下反应合成氨:N2+3H2 2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为C(N2)="0.100mol/L," C(H2)=0.300mol/L进行反应时, N2的浓度随时间的变化如下图①、②、③曲线所示。
2NH3 △H<0。某实验室在三个不同条件的密闭容器中,分别加入浓度均为C(N2)="0.100mol/L," C(H2)=0.300mol/L进行反应时, N2的浓度随时间的变化如下图①、②、③曲线所示。
(1)该反应平衡常数的数学表达式 ;实验②平衡时H2的转化率为_______
(2)据图所示,②、③两装置中各有一个条件与①不同。请指出,并说明判断的理由。
②条件:_______ 理由: ________
③条件:_______ 理由: ________
(16分)某混合物粉末可能含有Al、Fe、FeO、Al2O3,某研究小组在实验室积极探究其组成。
(1)研究小组首先排除了含有单质Al的可能性,加入的试剂是_______(填序号)
| A.硫酸 | B.盐酸 | C.氨水 | D.氢氧化钠溶液 |
证明不含单质铝的现象是 。
(2) 该混合物的组成基本确定为Fe、FeO、Al2O3。请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/L盐酸、3% H2O2、3mol/LCuSO4、蒸馏水。
根据你设计的实验方案,在答题卡上按下表的格式写出空白部分的实验操作、预期现象和结论。
| 实验操作 |
预期现象和结论 |
| 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。 |
粉末减少,说明粉末可能含有Al2O3 |
| 步骤2:取少量步骤1的滤液于试管中,逐滴滴加3mol/L盐酸至过量。 |
_____________________________, 说明粉末中含有Al2O3。 |
| 步骤3:将步骤1的滤渣转移到烧杯B中,加入足量3mol/L CuSO4,充分搅拌,过滤,洗涤。 |
有红色固体生成,说明粉末中含有____。 |
| 步骤4: |
|

 粤公网安备 44130202000953号
粤公网安备 44130202000953号