辽宁省本溪县高二上学期月考化学试题
下列说法中正确的是( )
| A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时, 反应为吸热反应 |
| C.为了提高煤的利用率,常将煤气化或直接液化后燃烧。煤气化或直接液化属于物理变化 |
| D.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0 |
强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H
=-57.3KJ·mol-1。分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是()
| A.△H1>△H2>△H3 | B.△H1<△H2<△H3 |
| C.△H1>△H2=△H3 | D.△H1=△H2<△H3 |
已知下列两个反应中:
4P(白磷,s)+5O2(g)=2P2O5(s) △H= -Q1 KJ/mol
4P(红磷,s)+5O2(g)=2P2O5(s) △H= -Q2 KJ/mol
且Q1>Q2,则不正确的是( )
| A.燃烧白磷放出的能量比燃烧红磷放出的能量多 |
| B.白磷转化为红磷是属于放热反应 |
| C.白磷和红磷互为同素异形体 |
| D.等质量的白磷和红磷,白磷含有的能量比红磷的低 |
在密闭容器中有可逆反应nA (g)+mB(g)  pC(g) △H>0 处于平衡状态(知n+m>p),下列说法正确的是()
pC(g) △H>0 处于平衡状态(知n+m>p),下列说法正确的是()
①升高温度时,c(B)/c(C)的比值减小 ②降温时,体系内混合气体平均式量减小
③加入B,A的转化率变大 ④加入催化剂,气体的总物质的量不变
⑤充入C,则A,B的物质的量增大
A ③④ B ①②⑤ C ②③⑤ D 全部
在一密闭容器中进行下列反应:2SO2+O2 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是 ( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是 ( )
| A.SO2为0.4mol/L,O2为0.2mol/L | B.SO2为0.25mol/L |
| C.SO2,SO3均为0.15mol/L | D.SO3为0.4mol/L |
下列说法中有明显错误的是( )
| A.对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大 |
| B.活化分子之间发生的碰撞不一定为有效碰撞 |
| C.升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| D.加入适宜的催化剂,使分子能量增加从而可使活化分子的百分数大大增加,从而成千上万倍地增大反应速率 |
某温度下,已知反应mX(g)+ nY(g)  qZ(g) △H=" +Q" kJ·mol—1(Q>0),下列叙述正确的是( )
qZ(g) △H=" +Q" kJ·mol—1(Q>0),下列叙述正确的是( )
| A.反应达到最大限度时,加入X,反应的△H增大 | |
| B.在一定条件下向容器中放入m molX和n mol Y,充分反应吸收Q kJ的能量 | |
C.反应速率υ正(X) = υ正(Y) υ正(Y) |
D.降低温度,反应的速率值变大 |
已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如右图。
N2O4(g) △H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如右图。 下列说法不正确的是( )
下列说法不正确的是( )
| A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线 |
| B.前10 min内用v(N2O4)表示的化学反应速率为0.02 mol/(L·min) |
| C.25 min时,NO2转变为N2O4的反应速率增大,其原因是将密闭容器的体积缩小为1L |
| D.前10 min内用v(NO2)表示的化学反应速率为0.04 mol/(L·min) |
一个真空密闭容器中盛有1molPCl5,加热到200℃时发生了反应:PCl5(g) PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M %,若在同一温度和同样容器中最初投入的是2molPCl5,反应达到平衡时PCl5的分解率为N %。M与N的关系是 ( )
PCl3(g)+Cl2(g),反应达到平衡时PCl5的分解率为M %,若在同一温度和同样容器中最初投入的是2molPCl5,反应达到平衡时PCl5的分解率为N %。M与N的关系是 ( )
| A.M>N | B.M<N | C.M=N | D.无法确定 |
在某容积一定的密闭容器中,可逆反应:A(g)+B(g) xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是 ( ).
xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是 ( ).
| A.p3>p4,Y轴表示A的质量 | B.p3<p4,Y轴表示B的百分含量 |
| C.p3>p4,Y轴表示混合气体密度 | D.p3>p4,Y轴表示混合气体平均摩尔质量 |
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。
(1)实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01 mol·L-1、0.001 mol·L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液(0.1 mol·L-1)的用量均为2mL。如果要探 究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成_______个实验进行对比即可得出结论。
究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成_______个实验进行对比即可得出结论。
(2)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
| KMnO4酸性溶液 的浓度 / mol·L-1 |
溶液褪色所需时间 t / min |
||
| 第1次 |
第2次 |
第3次 |
|
| 0.01 |
14 |
13 |
11 |
| 0.001 |
6 |
7 |
7 |
①计算用0.001 mol·L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率(忽略混合前后溶液的体积变化)。
②若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?____________。若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:
某同学发现在灼热的煤炭上洒少量水,煤炉中会产生淡蓝色火焰,煤炭燃烧更旺, 因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧放出更多的热量。”(已知煤炭的燃烧热为-393.15 kJ/mol,氢气的燃烧热为-242 kJ/mol,一氧化碳的燃烧热为-283 kJ/mol)
因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧放出更多的热量。”(已知煤炭的燃烧热为-393.15 kJ/mol,氢气的燃烧热为-242 kJ/mol,一氧化碳的燃烧热为-283 kJ/mol)
(1)写出该同学看到燃烧现象所涉及到的所有热化学反应方程式;
(2)你认为该同学的结论是否正确,请简要说明理由。
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):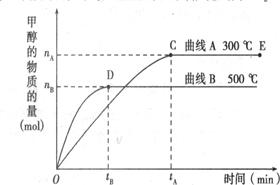
根据题意完成下列各题:
⑴反应达到平衡时,平衡常数表达式K=
升高温度,K值 (填“增大”“减小”或“不变”)。
⑵5000C ,从反应开始到平衡,氢气的平均反应速率v(H2)= (用nB、 tB 表示)
⑶在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,下列有关该体系的说法正确的是
a .氢气的浓度减少
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时n(H2)/n(CH3OH)增大
⑷可逆反应:CO(g)+ 2H2(g) CH3OH(g)在恒容密闭容器中反应,达到平衡状态的标志是:
CH3OH(g)在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成2n molH2的同时生成n mol CH3OH
②单位时间内生成2n molH2的同时,生成n mol CO
③用CO、H2、CH3OH 的物质的量浓度变化表示的反应速率的比为1 : 2 : 1的状态
④混合气体的密度不再改变的状态
⑤混合气体的平均相对分子质量不再改变的状态
⑸据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
 xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 试计算:
xC(气) + 2D(气),5 min后反应达到平衡状态,容器内的压强变小,已知D的平均反应速度为 0.1 mol/(L﹒min), 试计算: 粤公网安备 44130202000953号
粤公网安备 44130202000953号