北京市西城区高二下学期期末考试化学试题
下列关于石油的说法正确的是
| A.液化石油气、天然气都是可再生能源 | B.石油丰要含有碳、氢两种元素 |
| C.石油的裂化和裂解都属于物理变化 | D.石油分馏出的各馏分均是纯净物 |
某烷烃的结构简式为 ,它的正确命名是
,它的正确命名是
| A.4-甲-3-乙基戊烷 | B.3-丙基戊烷 |
| C.2-甲基-3-乙基戊烷 | D.3-乙基-2-甲基戊烷 |
能够快速、微量、精确的测定相对分子质量的物理方法是
| A.质谱 | B.红外光谱 | C.紫外光谱 | D.核磁共振谱 |
下列表述正确的是
A.醛基的结构简式 |
B.聚丙烯的结构简式 |
C.四氯化碳分子的电子式 |
D.丙烷分子的球棍模型 |
在下列各组物质中,属于同系物的是
| A.苯酚和苯 | B.甲烷和2,2-二甲基丁烷 |
| C.乙二醇和丙三醇 | D.1,1-二氯乙烷和l,2-二氯乙烷 |
比较下列各组物质的沸点①乙醇>丙烷②正丁烷>异丁烷③1-丁烯>1-庚烯,其中正确的是
| A.①② | B.①③ | C.②③ | D.①②③ |
下列物质可用重结晶法提纯的是
| A.含杂质的工业酒精 | B.含杂质的粗苯甲酸 |
| C.从溴水中提纯溴 | D.苯中混有少量苯酚 |
下列有关葡萄糖的说法正确的是
A.葡萄糖的分子式是 |
B.葡萄糖为多羟基酮 |
| C.葡萄糖能发生水解反应 | D.葡萄糖属于高分子化合物 |
下列关于乙炔制取的说法中,正确的是
A.实验室制取乙炔的反应为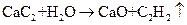 |
| B.为了加快反应速率可用饱和食盐水代替水 |
| C.点燃乙炔前必须验纯 |
| D.用高锰酸钾酸性溶液除乙炔中的杂质 |
下列有关生活常识的说法中,正确的是
A.棉、毛及合成纤维完全燃烧都只生成 和 和 |
| B.油脂变质后有难闻的气味是由于其发生了化学变化 |
| C.合成高分子材料都难以降解,会造成环境污染 |
| D.食品包装袋、食物保鲜膜等材料的主要成份是聚氯乙烯 |
用一种试剂鉴别乙醇、苯、1-己烯、苯酚溶液,可选用的试剂是
| A.浓溴水 | B.氯化铁溶液 | C.盐酸 | D.四氯化碳 |
某烃经催化加氢后,不能得到2-甲基丁烷,该烃是
| A.2-甲基-1-丁烯 | B.2-甲基-2-丁烯 |
| C.3-甲基-1-丁炔 | D.3,3-二甲基-1-丁炔 |
下列事实不能用有机物分子内基团间的相互作用解释的是
| A.乙烯能发生加成反应而乙烷不能 |
| B.苯酚能跟NaOH溶液反应而乙醇不能 |
C.甲苯能使 酸性溶液褪色而乙烷不能 酸性溶液褪色而乙烷不能 |
| D.苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可 |
下列叙述中,正确的是
| A.将硝酸银溶液滴入浓氨水中制银氨溶液 |
| B.蒸馏操作时应将温度计的水银球插入液面下 |
| C.如果不慎将苯酚沾到皮肤上,应立即用酒精洗涤 |
| D.向蔗糖溶液中加入几滴稀硫酸,水浴加热,然后向其中加入银氨溶液,观察到银镜 |
下列化学方程式正确的是
A.甲苯与浓硝酸反应 |
B.乙酸乙酯在酸性条件下水解 |
C.乙醛与新制氢氧化铜反应 |
| D.苯酚钠溶液中通入少量二氧化碳 |

巴豆酸的结构简式为 。现有①氯化氢②溴水③纯碱溶液④2-丁醇⑤高锰酸钾酸性溶液,在一定条件下可能与巴豆酸反应的是
。现有①氯化氢②溴水③纯碱溶液④2-丁醇⑤高锰酸钾酸性溶液,在一定条件下可能与巴豆酸反应的是
| A.只有②④⑤ | B.只有①③④ | C.只有①②@④ | D.①②③④⑤ |
实验室用右图所示的装置制取乙酸乙酯,下列说法正确的是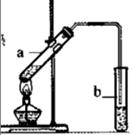
| A.试管a中先加入浓硫酸,再加入适量的乙醇和冰醋酸,然后加热 |
| B.试管b中加入氢氧化钠溶液除去乙酸乙酯中少量的乙酸和乙醇 |
| C.及时将乙酸乙酯蒸出,平衡向生成乙酸乙酯的方向移动 |
D.用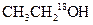 与乙酸反应制取酸乙酸乙酯, 与乙酸反应制取酸乙酸乙酯,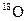 存在于水中 存在于水中 |
某有机物的结构简式为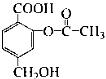 ,能与1 mol该化合物反应的NaOH的物质的量是
,能与1 mol该化合物反应的NaOH的物质的量是
| A.1 mol | B.2 mol | C.3 mol | D.4 mol |
“绿色化学”对化学反应提出了“原子经济性”(原子节约) 的概念及要求。理想的“原子经济性”反应中,原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合“原子经济性”的是
| A.苯乙烯在一定条件下制聚苯乙烯 | B.乙醇与浓硫酸共热制乙烯 |
| C.乙醇催化氧化制乙醛 | D.乙烷与氯气反应制氯乙烷 |
以2-溴丙烷为原料制取1,2-丙二醇,需要经过的反应是
| A.加成—消去一取代 | B.取代一消去—加成 |
| C.消去—取代一加成 | D.消去—加成—取代 |
(6分) 某有机物的结构简式为 ,请回答下列问题。
,请回答下列问题。
(1)该有机物的分子式是 。
(2)该有机物所含官能团的名称是 、 。
(3)该有机物与氢氧化钠溶液反应,其产物的结构简式是 。
(4)对该有机物性质的描述中,正确的是 (填写选项的字母)。
a.能与 溶液反应 b.具有两性 c.能发生水解反应
溶液反应 b.具有两性 c.能发生水解反应
(14分) 下图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精。已知D在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家石油化工发展水平。E是生活中常见的一种有机物。各物质间转化关系如下:
请回答下列问题。
(1)A的名称是 。
(2)B中所含的官能团是 。
(3)C+E X的化学反应类型是 反应。
X的化学反应类型是 反应。
(4)写出任意两种与A具有相同官能团的A的同分异构体的结构简式(不含A):
、 。
(5)X与氢氧化钠溶液反应的化学方程式是
。
(6)以D为原料生产一种常见塑料的化学方程式是
。
(每空1分,共7分)溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是 。
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下: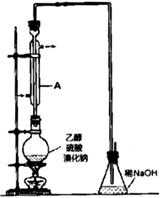
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有 生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。
生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确选项的字母)。
a.饱和食盐水 b.稀氢氧化钠溶液 c.乙醇 d.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
(4)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水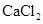 ,然后进行的实验操作是 (填写正确选项的字母)。
,然后进行的实验操作是 (填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(5)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入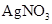 溶液 ③加入稀
溶液 ③加入稀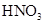 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液
(8分) 某有机物A的相对分子质量为62。为进一步测定A的化学式,现取6.2 gA完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重
5.4 g和8.8 g (假设每步反应完全)。
(1)该有机物的实验式是 :分子式是 。
(2)红外光谱显示有“C—C”键和“O一H”键的振动吸收,若核磁兆振氢谱有2个吸收峰,峰面积之比为1:2,推断该有机物的结构简式是 。
(3)该有机物与金属钠反应的化学方程式是 。
(10分) 肉桂酸是重要的有机合成中间体,广泛用于医药、香料、塑料和感光树脂等化工产品中。肉桂酸的结构简式为
请回答下列问题。
(1)肉桂酸的分子式是 。
(2)写出肉桂酸的顺式结构 。
(3)肉桂酸与乙醇在一定条件下发生反应的化学方程式是
。
(4)已知:
由苯甲醛制备肉桂酸的合成路线如下:
①上述合成路线中,反应I中氧化剂可选择 (填写正确选项的字母)。
a.高锰酸钾酸性溶液 b.新制氧氧化铜 c.溴的四氯化碳溶液
②苯甲醛与有机物X反应生成A的化学方程式是
。
(10分) 化合物A经李比希法和质谱法分析得知其分子式是 ,相对分子质量136。A的核磁共振氧谱有4个峰,峰面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有个取代基,其核磁共振氢谱与红外光谱如下图。
,相对分子质量136。A的核磁共振氧谱有4个峰,峰面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有个取代基,其核磁共振氢谱与红外光谱如下图。
请回答下列问题。
(1)A的结构简式是 。
(2)A的同分异构体(不含A) 中属于酯类的芳香族化台物共有 种,请写出其
中任意两种的结构简式 、 。
(3)B与A互为同分异构体且能与碳酸氢钠反应,B的核磁共振氢谱也有4个峰,峰面
积之比为1:2:2:3,请参照示例写出以B和乙烯为原料在一定条件下台成聚酯 的合成路线。
的合成路线。
示例:











 C的化学方程式是
C的化学方程式是 粤公网安备 44130202000953号
粤公网安备 44130202000953号