2010年高考化学试题分项专题七 化学反应中的能量变化
下列各表述与示意图一致的是

| A. | 图①表示25 时,用0.1 盐酸滴定20 0.1 溶液,溶液的 随加入酸体积的变化 |
| B. |
图②中曲线表示反应
 ;
正、逆反应的平衡常数K随温度的变化
;
正、逆反应的平衡常数K随温度的变化
|
| C. | 图③表示10 0.01 酸性溶液与过量的0.1 溶液混合时, 随时间的变化 |
| D. | 图④中 曲线分别表示反应 ; 使用和未使用催化剂时,反应过程中的能量变化 |
、、、、五种元素的原子序数依次增大。、、、是组成蛋白质的基础元素,是地壳中含量最高的金属元素。
回答下列问题:
⑴ 的元素符号为 ;在元素周期表中的位置为;五种元素的原子半径从大到小的顺序是(用元素符号表示)。
⑵ 、两元素按原子数目比l∶3和2∶4构成分子和,的电子式为,的结构式为。
⑶ 硒()是人体必需的微量元素,与同一主族,原子比原子多两个电子层,则的原子序数为,其最高价氧化物对应的水化物化学式为。该族2 ~ 5周期元素单质分别与反应生成l气态氢化物的反应热如下,表示生成1硒化氢反应热的是(填字母代号)。
a.+99.7 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
⑷ 用单质 作阳极,石墨作阴极,溶液作电解液进行电解,生成难溶物,受热分解生成化合物 。写出阳极生成的电极反应式;由生成的化学方程式:。
作阳极,石墨作阴极,溶液作电解液进行电解,生成难溶物,受热分解生成化合物 。写出阳极生成的电极反应式;由生成的化学方程式:。
、、、是元素周期表前四周期中的四种常见元素,其相关信息如下表;
| 元素 |
相关信息 |
| 的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
| 常温常压下,单质是淡黄色固体,常在火山口附近沉积 |
|
| 和同周期,的电负性大于 | |
| 的一种核素的质量数为63,中子数为34 |
(1) 位于元素周期表第周期第)族,和最高价氧合物对应的水化物的酸性较强的是(化学式)
(2是一种常用的溶剂,的分子中存在个键。在,两种共价键中,键的极性较强的是,键长较长的是。
(3)的基态原子核外电子排布式是。在空气中煅烧生成的化学方程式是。
(4)处理含验到气污染的一种方法,是将其在催化剂作用下转化为单质。
已知:
此反应的热化学方程式是
下列说法不正确的是
| A. | 铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B. | 常温下,反应 不能自发进行,则该反应的 |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D. | 相同条件下,溶液中 、 、 的氧化性依次减弱 |
下表列出了3种燃煤烟气脱硫方法的原理。

(1)方法Ⅰ中氨水吸收燃煤烟气中的化学反应为:


能提高燃煤烟气中去除率的措施有(填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D . 通入空气使转化为
. 通入空气使转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的,原因是(用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:




与反应生成的热化学方程式为。
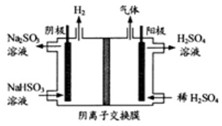
(3)方法Ⅲ中用惰性电极电解溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
下列判断正确的是
| A. | 测定硫酸铜晶体中结晶水含量时,灼烧至固体发黑,测定值小于理论值 |
| B. | 相同条件下,2 氢原子所具有的能量小于1 氢分子所具有的能量 |
| C. | 0.1 的碳酸钠溶液的 大于0.1 的醋酸钠溶液的 |
| D. | 1 1 的碳酸钠溶液吸收 的量大于1L 硫化钠溶液吸收 的量 |
据报道,在300℃、70下由二氧化碳和氢气合成乙醇已成为现实。下列叙述错误的是
| A. | 使用 催化剂可大大提高生产效率 |
| B. | 反应需在300℃进行可推测该反应是吸热反应 |
| C. | 充入大量 气体可提高 的转化率 |
| D. | 从平衡混合气体中分离出 和 可提高 和 的利用率 |
接触法制硫酸工艺中,其主反应在并有催化剂存在下进行:
1)该反应所用的催化剂是(填写化合物名称),该反应时的平衡常数时的平衡常数(填"大于"、"小于"或"等于").
2)该热化学反应方程式的意义是.
3)达到化学平衡状态的是
a. b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入和,半分钟后达到平衡,测得容器中含,则:若继续通入和,则平衡移动(填"向正反应方向"、"向逆反应方向" 或"不"),再次达到平衡后,mol<<mol。
、、、、是原子序数依次增大的短周期主族元素,、在周期表中的相对位置如右表;元素最低负化合价的绝对值与其原子最外层电子数相等;是地壳中含量最多的金属元素。
(1)的离子结构示意图为;元素在周期表中位于第族。
(2)和氢组成的化合物分子有6个原子,其结构简式为。
(3)和形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为
(4)的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂的清除剂,所发生反应的产物不污染环境,其化学方程式为。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(>0)并达平衡后,仅改变下表中反应条件,该平衡体系中随递增递减的是(选填序号)。
| 选项 |
||||
| 温度 |
温度 |
加入的物质的量 |
加入甲的物质的量 |
|
| 甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由、形成的液态化合物0.2在中完全燃烧,生成两种气态氧化物,298时放出热量215。 该反应的热化学方程式为。
在298、100时,已知:
;
;
;
则与和间的关系正确的是:
| A. |
=+2 |
B. |
=+ |
| C. |
=-2 |
D. |
=- |
硼酸在食品、医药领域应用广泛。
(1)请完成气体与水反应的化学方程式:+ = +。
(2)在其他条件相同时,反应+ +中,3的转化率在不同温度下随反应时间的变化见图12,由此图可得出:
+中,3的转化率在不同温度下随反应时间的变化见图12,由此图可得出:

①温度对应该反应的反应速率和平衡移动的影响是_
②该反应的0(填"<"、"="或">").
(3)溶液中存在如下反应:
()+() -( )++()已知0.70 -1 溶液中,上述反应于298达到平衡时,(+)="2." 0 × 10-5-1,()≈(),水的电离可忽略不计,求此温度下该反应的平衡常数()的平衡浓度不列入的表达式中,计算结果保留两位有效数字)
-( )++()已知0.70 -1 溶液中,上述反应于298达到平衡时,(+)="2." 0 × 10-5-1,()≈(),水的电离可忽略不计,求此温度下该反应的平衡常数()的平衡浓度不列入的表达式中,计算结果保留两位有效数字)
下列与化学反应能量变化相关的叙述正确的是
| A. | 生成物能量一定低于反应物总能量 |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 |
| C. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D. | 同温同压下, (在光照和点燃条件下的 不同 |
已知 蒸发1需要吸收的能量为30,其它相关数据如下表:

则表中为
| A. | 404 | B. | 260 | C. | 230 | D. | 200 |
 粤公网安备 44130202000953号
粤公网安备 44130202000953号