高三化学第五套
下列制作铅笔的材料与相应工业不对应的是
| A.橡皮擦——橡胶工业 | B.铝合金片——冶金工业 |
| C.铝笔芯——电镀工业 | D.铅笔漆——涂料工业 |
下列关于有机化合物的说法正确的是
| A.聚氯乙烯分子中含碳碳双键 |
| B.以淀粉为原料可制取乙酸乙酯 |
| C.丁烷有3种同分异构体 |
| D.油脂的皂化反应属于加成反应 |
某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
| A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-="==" Cl-+ ClO-+ H2O |
B.该消毒液的pH约为12:ClO-+ H2O HClO+ OH- HClO+ OH- |
| C.该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O |
| D.该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-=" HClO+" CH3COO— |
下列实验操作正确且能达到相应实验目的的是
| |
实验目的 |
实验操作 |
| A |
称取2.0gNaOH固体 |
先在托盘上各放一张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
| B |
配制FeCl3溶液 |
将FeCl3固体溶解于适量蒸馏水 |
| C |
检验溶液中是否含有NH4+ |
取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| D |
验证铁的吸氧腐蚀 |
将铁钉放入试管中,用盐酸浸没 |
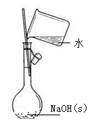
下列有关实验的选项正确的是
| A.配制0.10mol/L NaOH溶液 |
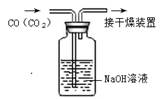
B.除去CO中的CO2 |
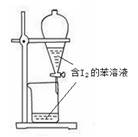
C.苯萃取碘水中的I2分出水层后的操作 |
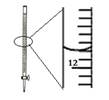
D.记录滴定终点读数为12.20mL |
 |
 |
 |
 |
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
下列说法中正确的是
| A.CO和O生成CO2是吸热反应 |
| B.在该过程中,CO断键形成C和O |
| C.CO和O生成了具有极性共价键的CO2 |
| D.状态Ⅰ →状态Ⅲ表示CO与O2反应的过程 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是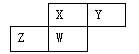
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:X>W>Z |
| C.最简单气态氢化物的热稳定性:Y>X>W>Z |
| D.元素X、Z、W的最高化合价分别与其主族序数相等 |
下列有关说法正确的是
| A.在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 |
| B.Fe(OH)3胶体无色、透明,能发生丁达尔现象 |
| C.H2、SO2、CO2三种气体都可用浓硫酸干燥 |
| D.SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 |
下列关于自然界中氮循环(如图)的说法不正确的是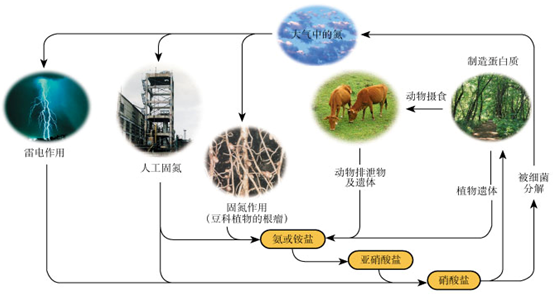
| A.氮元素均被氧化 |
| B.工业合成氨属于人工固氮 |
| C.含氮无机物和含氮有机物可相互转化 |
| D.碳、氢、氧三种元素也参与了氮循环 |
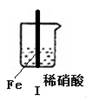
在通风橱中进行下列实验:
| 步骤 |
 |
 |
|
| 现象 |
Fe表面产生大量无色气泡,液面上方变为红棕色 |
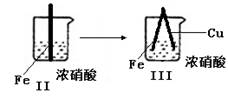
Fe表面产生少量红棕色气泡后,迅速停止 |
Fe、Cu接触后,其表面产生红棕色气泡 |
下列说法中不正确的是
A.Ⅰ种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
合成导电高分子材料PPV的反应: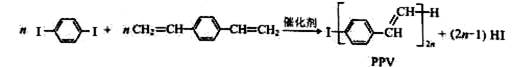
下列说法中正确的是
| A.合成PPV的反应为加聚反应 |
| B.PPV与聚苯乙烯具有相同的重复结构单元 |
C.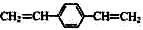 和苯乙烯互为同系物 和苯乙烯互为同系物 |
| D.通过质谱法测定PPV的平均相对分子质量,可得其聚合度 |
汽车尾气中,产生NO的反应为:N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是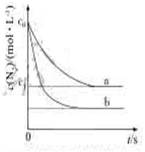
A.温度T下,该反应的平衡常数K=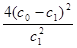 |
| B.温度T下,随着反应的进行,混合气体的密度减小 |
| C.曲线b对应的条件改变可能是加入了催化剂 |
| D.若曲线b对应的条件改变是温度,可判断该反应的△H<0 |
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是
| A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O) |
| B.加入10mL盐酸时:c(NH4+) +c(H+) = c(OH-) |
| C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+) |
| D.加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+) |
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是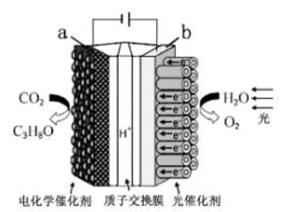
| A.该装置将化学能转化为光能和电能 |
| B.该装置工作时,H+从b极区向a极区迁移 |
| C.每生成1molO2,有44gCO2被还原 |
| D.a电极的反应为:3CO2+16H+-18e-=C3H8O+4H2O |
研究硫元素及其化合物的性质具有重要意义。
(1)①硫离子的结构示意图为 。
②加热时,硫元素的最高价氧化物对应水化物的浓溶液与木炭反应的化学方程式为 ______ 。
(2)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。
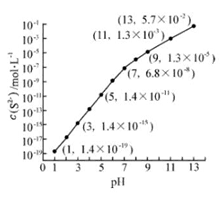
①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1.
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(3)25℃,两种酸的电离平衡常数如下表。
| |
Ka1 |
Ka2 |
| H2SO3 |
1.3×10-2 |
6.3×10-4 |
| H2CO3 |
4.2×10-7 |
5.6×10-11 |
①HSO3-的电离平衡常数表达式K= 。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为 。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为 。
(15分)无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为 。
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:

已知:
| 物质 |
SiCl4 |
AlCl3 |
FeCl3 |
FeCl2 |
| 沸点/℃ |
57.6 |
180(升华) |
300(升华) |
1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是 (只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是 。
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1="+1344.1kJ" ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2="+1169.2kJ" ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为 。
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为 ________。
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是 。
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水利用下图所示的实验装置进行实验。
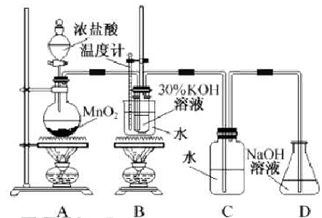
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有______。
(2)若对调B和C装置的位置,_____(填“能”或 “不能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3 。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
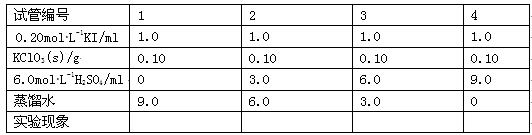
①系列a实验的实验目的是_______。
②设计1号试管实验的作用是___________。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为_________________。
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用右图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是_______(不考虑实验装置及操作失误导致不可行的原因)。
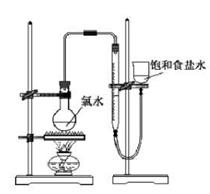
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):______
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学通过改变浓度研究“2Fe3++2I- 2Fe2++I2”反应中Fe3+和Fe2+的相互转化。实验如下:
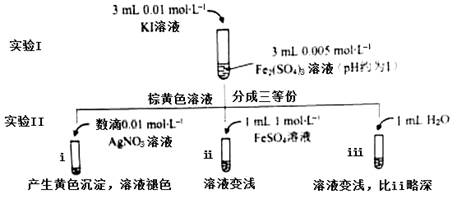
(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到 。
(2)iii是ii的对比试验,目的是排除有ii中 造成的影响。
(3)i和ii的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化。用化学平衡移动原理解释原因: 。
(4)根据氧化还原反应的规律,该同学推测i中Fe2+向Fe3+转化的原因:外加Ag+使c(I-)降低,导致I-的还原性弱于Fe2+,用下图装置(a、b均为石墨电极)进行实验验证。
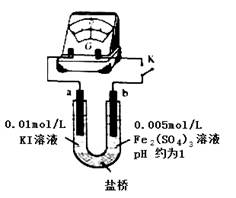
①K闭合时,指针向右偏转,b作 极。
②当指针归零(反应达到平衡)后,向U型管左管滴加0.01 mol/L AgNO3溶液,产生的现象证实了其推测,该现象是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号