上海市嘉定、黄浦区高三第二次模拟考试化学试题
运用化学知识可以解决日常生活中遇到的许多问题,下列说法不正确的是
| A.食用松花蛋时蘸些食醋可以去除氨味 |
| B.用双氧水的稀溶液清洗伤口可以杀菌消毒 |
| C.用淀粉溶液检验某食盐是否为加碘盐 |
| D.长期使用含氟牙膏可预防龋齿 |
钢铁生锈过程的反应为:①2Fe+O2+2H2O→2Fe(OH)2②4F e(OH)2+O2+2H2O→4Fe(OH)3 ③2Fe(OH)3→Fe2O3+3H2O,下列说法错误的是
e(OH)2+O2+2H2O→4Fe(OH)3 ③2Fe(OH)3→Fe2O3+3H2O,下列说法错误的是
| A.上述反应均为氧化还原反应 |
| B.反应①、②中氧化剂都是氧气 |
| C.与铜质水龙头连接处的钢质水管易发生腐蚀 |
| D.钢铁在潮湿的空气中通常发生吸氧腐蚀 |
下列说法不正确的是
| A.蛋白质水解的最终产物是氨基酸 |
| B.油脂水解生成甘油和高级脂肪酸或高级脂肪酸盐 |
| C.淀粉水解的最终产物是葡萄糖 |
| D.重油裂解可以得到汽油 |
下列实验环节错误的是
| A.块状固体药品的取用:一横、二放、三慢竖 |
| B.液体药品的倾倒:瓶塞倒放、紧挨瓶口、缓慢倒入 |
| C.分液的操作:静置分层后将分液漏斗中下层液从下口放出,再将上层液从上口倒出 |
| D.冷凝管的使用:冷却水下口进,上口出 |
化合物FeO具有NaCl型结构。在天然样品中,往往由于部分Fe2+被Fe3+代替,晶体存在缺陷,使n(Fe)︰n(O)<1。用Fe2+和Fe3+可以将组成为Fe0.95O的某天然FeO样品表示为
| A.Fe2+0.45Fe3+0.50O | B.Fe2+0.85Fe 3+0.10O |
| C.Fe2+0.15Fe3+0.80O | D.Fe2+0.20Fe 3+0.75º |
下列物质分类的正确组合是
| 分类 组合 |
碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
| A |
纯 碱 |
乙二酸 |
胆矾 |
氧化铝 |
二氧化碳 |
| B |
烧 碱 |
石炭酸 |
小苏打 |
氧化镁 |
一氧化碳 |
| C |
苛性钾 |
硬脂酸 |
萤石 |
过氧化钠 |
二氧化硫 |
| D |
苛性钠 |
油酸 |
苏打 |
氧化钠 |
三氧化硫 |
如右图所示,a、b是两根石墨棒,下列叙述错误的是
| A.往滤纸上滴加酚酞试液,a极附近颜色变红 |
| B.锌电极上的反应:Zn-2e→Zn2+ |
| C.稀硫酸中硫酸根离子的物质的量不变 |
| D.a是阳极,发生氧化反应 |
已知C3N4 晶体具有比金刚石还大的硬度,且原子间均以单键结合。下列关于C3N4晶体的 说法正确的是
说法正确的是
| A.C3N4晶体是分子晶体 |
| B.C3N4晶体中微粒间通过离子键结合 |
| C.C3N4晶体中C-N键的键长比金刚石中C-C键的键长要长 |
| D.C3N4晶体中每个C原子连接4个N 原子,而每个N原子连接3个C原子 |
下列各组顺序的排列不正确的是
| A.离子半径:F->Mg2+>Al3+ | B.热稳定性:HCl>H2S>AsH3 |
| C.酸性:H3AlO3<H2CO3<H3PO4 | D.水溶性:SO2< H2S< NH3 |
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以产生Cl2,下列关于混盐CaOCl2的有关判断不正确的是
| A.该混盐的水溶液呈碱性 |
| B.该混盐具有较强的氧化性 |
| C.该混盐中氯元素的化合价为零 |
| D.该混盐与硫酸反应产生71gCl2时转移1mol 电子 |
实验室有一瓶久置的白色粉末,元素分析证明它由钾、硫、氧三种元素组成,钾和硫的质量比为39∶16,下列结论正确的是
| A.根据元素分析结果推测该粉末为纯净物 |
| B.将粉末溶于水,加入氯化钡,观察到有白色沉淀生成,证明原粉末是硫酸钾 |
| C.将粉末加入盐酸中,产生气泡,证明原粉末是亚硫酸钾 |
| D.将粉末溶于水,加入氯化钡和盐酸,观察到有白色沉淀和气泡生成,原粉末可能是硫酸钾和亚硫酸钾的混合物 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,该集气瓶中的气体可能是
① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④ N2、H2
| A.①② | B.②③ | C.②④ | D.③④ |
将石墨置于熔融的钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是C8K、C24K、C36K、C48K和C60K。在钾石墨中,钾元素处于石墨中间层,因而石墨层之间被胀大,层间距离增大,钾原子把最外层电子交给石墨层但在遇到与金属钾易反应的其它物质时还会收回。下列对钾石墨的叙述正确的是
| A.钾石墨是一类共价化合物 | B.钾石墨导电性比石墨强 |
| C.钾石墨遇水不产生氢气 | D.C8K、C24K和C36K属于同素异形体 |
2008年诺贝尔化学奖授予美籍华裔钱永健等三位科学家,以表彰他们发现和研究了绿色荧光蛋白。荧光素是发光物质的基质,5-羧基荧光素(5-FAM)结构简式如右图所示,在碱性条件下有强烈的绿色荧光,广泛应用于荧光分析等。下列有关5-FAM说法不正确的是
| A.可与碳酸氢钠溶液反应 |
| B.分子式为C21H12O7 |
| C.1mol 该物质与足量NaOH溶液反应,可消耗4 mol氢氧化钠 |
| D.不与FeCl3发生反应 |
用下图装置测定水中氢、氧元素的质量比,方法是分别测定通氢气前后玻璃管的质量差和U型管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,不正确的是
| A.Ⅰ、Ⅱ装置之间缺少干燥装置 | B.Ⅱ装置中玻璃管内有水冷凝 |
| C.Ⅱ装置中CuO没有全部被还原 | D.Ⅲ装置后缺少干燥装置 |
加入铝粉能放出H2的溶液中肯定不能大量共存的离子组是
A. Fe3+、NO 、Cl-、NH
、Cl-、NH B.Ba2+、Mg2+、NO
B.Ba2+、Mg2+、NO 、Cl-
、Cl-
C.SO 、Cl-、K+、NH
、Cl-、K+、NH D.SO
D.SO 、K+、AlO
、K+、AlO 、Na+
、Na+
用NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.1NA |
| B.标准状况下,2.24L乙烷含有的化学键总数为0.8NA |
| C.常温下,23gNO2和N2O4的混合气体中含有的氮原子数为0.5 NA |
| D.标准状况下,22.4L甲醇中含有的氧原子数为NA |
下列反应的离子方程式正确的是
| A.硫化亚铁中加入稀硫酸 2H++S2-→H2S↑ |
B.向苯酚钠溶液中通入少量的CO2 -O-+CO2+H2O→ -O-+CO2+H2O→ -OH+HCO -OH+HCO |
C.向碳酸氢钠溶液中滴入少量石灰水 HCO +Ca2++OH-→CaCO3↓+H2O +Ca2++OH-→CaCO3↓+H2O |
D.向明矾溶液中加入过量的氨水 A13++3NH3·H2O→Al(OH)3↓+3NH |
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH 、Ba2+、Cl-、CO
、Ba2+、Cl-、CO 、SO
、SO 。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH 可能存在 可能存在 |
B.CO 一定存在 一定存在 |
| C.Na+一定存在 | D.一定不存在Cl- |
五种短周期元素的性质或原子结构信息如下表:
| 元素 |
元素性质或原子结构信息 |
| Q |
原子核外有6种不同运动状态的电子 |
| R |
最外层电子数是次外层电子数的3倍 |
| X |
气态氢化物的水溶液 呈弱碱性 呈弱碱性 |
| Y |
第三周期元素的简单离子中离子半径最小 |
| Z |
单质为银白色固体,在空气中燃烧发出黄色火焰 |
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有 。
(2)R与Z组成的化合物的化学式是 。
(3)X气态氢化物分子的空间构型为 。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有 。
(4)Y单质与V2O5反应的化学方程式为 。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为 。
某反应体系中反应物与生成物有:K2SO4、CaSO4、MnSO4、CaC2O4、KMnO4、H2SO4、H2O和一种未知气体X。
(1)已知CaC2O4在反应中失去电子,则该反应的氧化剂是 。
(2)在标准状况下生成11.2LX时,有0.5mol 电子转移,共消耗0.25mol CaC2O4,X的化学式为 。
(3)将氧 化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
(4)反应中CaC2O4表现 性,发生 反应,生成 产物(选填“氧化”或“还 原”),氧化还原反应的本质是 。
原”),氧化还原反应的本质是 。
工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但钾却不能用电解熔融KCl的方法制得,因金属钾易溶于熔融态的KCl中而有危险,难获得钾,且降低电流效率。现生产钾是用属钠和熔化的KCl在一定的条件下反应制取:
有关数据如下表:
| |
熔点℃ |
沸点℃ |
密度(g/cm3) |
| Na |
97.8 |
882.9 |
0.97 |
| K |
63.7 |
774 |
0.86 |
| NaCl |
801 |
1413 |
2.165 |
| KCl |
770 |
1500(升华) |
1.984 |
(1)工业上制取金属钾的化学原理是 ,在常压下金属钾转为气态从反应混合物中分离的最低温度约为 ,而反应的最高温度应低于 。
(2)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是 。
(3)生产中常向反应物中通入一种气体,并将从反应器中导出的气体进行冷却得到金属钾,且将该气体可循环利用,该气体是________。
a.干燥的空气 b.氮气 c.二氧化碳 d.稀有气体
(4)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为K= 。
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)利用B装置可制取的气体有 。
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
①若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的产物有漂白性 |
| Ⅱ |
氯水中加入 NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由。
 。
。
②请利用上述装置设计一个简单的实验,验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
 。
。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2
并进行有关实验。
① B中发生反应的化学方程式为 。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 。
③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是 (气体按标准状况计算)。
氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂和生产含氟牙膏等。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:
有关物质在水中溶解度(g/100gH2O)如下:
| 温度 |
10℃ |
20℃ |
30℃ |
溶解度:20℃NaF—4 0℃NH4F—100; 常温Na2SiF6微溶于水 |
| NH4Cl溶解度 |
33.3 |
37.2 |
41.4 |
请回答下列问题:
(1)操作Ⅰ需要用到的玻璃仪器有  。
。
(2)上述流程中发生两步反应,化学方程式为 ,
。
(3)操作II的作用是 ,
操作Ⅲ的具体过程是 。
(4)流程中NH4HCO3必须过量,其原因是
_______________________________________________________________________。
已知G的分子结构模型如右图所示(图中球与球之间连线表示单键或双键),用芳香烃A为原料合成G的路线如下:
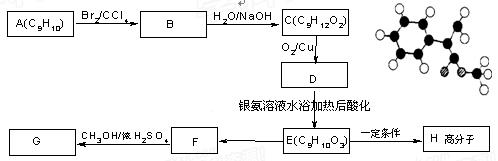
试回答下列问题:
(1)G的结构简式为 ,G的一种同分异构体的结构简式为 。
(2)化合物E中的含氧官能团有 (填名称)。
(3)A→B的反应类型是 ,E→F的反应类型是 。
(4)书写 化学方程式
化学方程式
C→D
E→H
不对称烯烃与HX发生加成反应时HX中的H原子加成到含H较多的碳原子上。俄国化学家马科尼可夫因提出不对称烯烃的加成规则而著称于世。
又知:①CH3CH2Br+NaCN CH3CH2CN+NaBr
CH3CH2CN+NaBr
②CH3CH2CN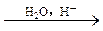
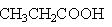
③CH3CH2COOH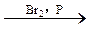 CH3CHBrCOOH
CH3CHBrCOOH
有下列有机物之间的相互转化: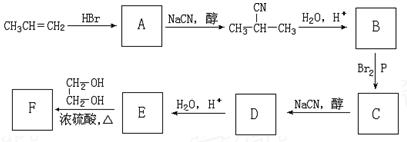
回答下列问题:
(1)B→C的反应类型为 ;
(2)C→D、E→F的化学方程式为:
C→D ,
E→F(F为高分子时) 。
(3)F可以有多种结构,写出下列情况下F的结构简式:
①分子式为C7H12O5 ,②分子内含有一个七元环 。
氯化亚铜(CuCl)是重要的化工原料。工业上常通过下列反应制备CuCl:
2CuSO4+Na2SO3+2NaCl+Na2CO3→2CuCl↓+3Na2SO4+CO2↑
(1)CuCl制备过程中需要配制质量分数为20.0%的CuSO4溶液,配制该溶液所需的CuSO4·5H2O与H2O的质量之比为 。
(2)准确称取所配制的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1的Ce(SO4)2溶液滴定到终点,消耗24.60mLCe(SO4)2溶液。有关反应的离子方程式为:
Fe3++CuCl→Fe2++Cu2++Cl- Ce4++Fe2+→Fe3++Ce3+
已知国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.50%。试通过计算说明上述样品中CuCl的质量分数是否符合国家标准。
为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4。为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
| 实验序号 |
样品的质量/g |
NaOH溶液的体积/mL |
氨气的 体积/L 体积/L |
| Ⅰ |
7.4 |
40.00 |
1.68 |
| Ⅱ |
14.8 |
40.00 |
3.36 |
| Ⅲ |
22.2 |
40.00 |
1.12 |
| Ⅳ |
37.0 |
40.00 |
0 |
(1)测定过程中有关反应的离子方程式为
_____________________________ 。
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为__________L。
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4)欲计算该NaOH溶液的物质的量浓度应选择第______组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号