2009高考真题汇编—有机综合题
环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:

环己醇、环己酮和水的部分物理性质见下表:
| 物质 |
沸点(℃) |
密度(,20℃) |
溶解性 |
| 环己醇 |
161.1(97.8)★ |
0.9624 |
能溶于水 |
| 环己酮 |
155.6(95)★ |
0.9478 |
微溶于水 |
| 水 |
100.0 |
0.9982 |
★括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性溶液氧化环己醇反应的,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性溶液的加料方式为。
②蒸馏不能分离环己酮和水的原因是。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水固体,除去有机物中的少量水。
①上述操作的正确顺序是(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需。
③在上述操作c中,加入 固体的作用是。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有种不同化学环境的氢原子。
一种从植物中提取的天然化合物,可用于制作"香水",其结构为:

 ,
,
有关该化合物的下列说法不正确的是()
| A. |
分子式为 |
| B. |
该化合物可发生聚合反应 |
| C. |
1该化合物完全燃烧消耗19 |
| D. |
与溴的溶液反应生成的产物经水解、稀硝酸化后可用溶液检验 |
各物质之间的转换关系如下图,部分生成物省略。、是由、、中两种元素组成的化合物,、、的原子序数依次增大,在周期表中的原子半径最小,、原子量外层电子数之和为10。为无色非可燃性气体,为黄绿色单质气体,、为金属,有漂白作用,反应①常用于制作印刷电路板。



 请回答下列问题:
请回答下列问题:
 (1)写出的化学式, 的电子式。
(1)写出的化学式, 的电子式。
 (2)比较与的原子半径大小> (填写元素符号)。
(2)比较与的原子半径大小> (填写元素符号)。
 (3)写出反应②的化学方程式(有机物用结构简式表示),举出该反应的一个应用实例。
(3)写出反应②的化学方程式(有机物用结构简式表示),举出该反应的一个应用实例。
 (4)已知溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式。
(4)已知溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式。
 (5)研究表明:气体在一定条件下可被还原为晶莹透明的晶体,其结构中原子的排列为正四面体,请写出及其2种同素异形体的名称、、。
(5)研究表明:气体在一定条件下可被还原为晶莹透明的晶体,其结构中原子的排列为正四面体,请写出及其2种同素异形体的名称、、。
苄佐卡因时一中医用麻醉药品,学名对氨基苯甲酸乙酯,它以对硝基甲苯为主要起始原经下列反应制得:



请回答下列问题:
 (1)写出、、的结构简式::、、。
(1)写出、、的结构简式::、、。
 (2)用核磁共振谱可以证明化合物中有种氢气、处于不同的化学环境。
(2)用核磁共振谱可以证明化合物中有种氢气、处于不同的化学环境。
 (3)写出同时符合下列要求的化合物的所有同分异构体的结构简式(除外)
(3)写出同时符合下列要求的化合物的所有同分异构体的结构简式(除外)
 ①化合物是1,4-二取代苯,期中苯环上的一个取代基是硝基
①化合物是1,4-二取代苯,期中苯环上的一个取代基是硝基
 ②分子中含有
②分子中含有 结构的基因
结构的基因
 注:结构如下:
注:结构如下:



(4)中有一化合物经酸性水解,期中的一种产物能与溶液发生显色反应,写出该水解反应的化学方程式。
 (5)苄佐卡因()的水解反应如下:
(5)苄佐卡因()的水解反应如下:



化合物经聚合反应可制成高分子纤维,广泛用于通讯、导弹、宇航等领域。请写出该聚合反应的化学方程式。
四川汶川盛产品质优良的甜樱桃。甜樱桃中含有一种羟基酸(用表示),的碳链结构无支链,化学式为;1.34 g 与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。在一定条件下可发生如下转化:




 其中,、、、分别代表一种直链有机物,它们的碳原子数相等。的化学式为(转化过程中生成的其它产物略去)。
其中,、、、分别代表一种直链有机物,它们的碳原子数相等。的化学式为(转化过程中生成的其它产物略去)。
 已知:
已知:


的合成方法如下:
①


②
其中,、、分别代表一种有机物。
 请回答下列问题:
请回答下列问题:
 (1)的结构简式是。
(1)的结构简式是。
 (2)生成的化学方程式是。
(2)生成的化学方程式是。
 (3)与乙醇之间发生分子间脱水,可能生成的有机物共有种。
(3)与乙醇之间发生分子间脱水,可能生成的有机物共有种。
 (4)的结构简式是。
(4)的结构简式是。
 (5)写出与水反应生成和的化学方程式:。
(5)写出与水反应生成和的化学方程式:。
 新型锂离子电池在新能源的开发中占有重要地位。可用作节能环保电动汽车的动力电池。磷酸亚铁锂()是新型锂离子电池的首选电极材料,它的制备方法如下:
新型锂离子电池在新能源的开发中占有重要地位。可用作节能环保电动汽车的动力电池。磷酸亚铁锂()是新型锂离子电池的首选电极材料,它的制备方法如下:
 方法一:将碳酸锂、乙酸亚铁[]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
方法一:将碳酸锂、乙酸亚铁[]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出。
 方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀。沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂。
 在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子选移的介质,该有机聚合物的单体之一(用表示)的结构简式如下:
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子选移的介质,该有机聚合物的单体之一(用表示)的结构简式如下:


 请回答下列问题:
请回答下列问题:
 (1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是。
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行。其原因是。
 (2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有、
(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有、 、(填化学式)生成。
、(填化学式)生成。
 (3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为 。
。
 (4)写出M与足量氧化钠溶液反应的化学方程式:
(4)写出M与足量氧化钠溶液反应的化学方程式: 。
。
 (5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为。
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为。
均为有机化合物,它们之间的转化如下图所示:


实验表明:①既能发生银镜反应,又能与金属钠反应放出氢气:
 ②核磁共振氢谱表明分子中有三种氢,且其峰面积之比为1:1:1;
②核磁共振氢谱表明分子中有三种氢,且其峰面积之比为1:1:1;
 ③能使溴的四氯化碳溶液褪色;④1与足量金属钠反应可放出22.4氢气(标准状况)。
③能使溴的四氯化碳溶液褪色;④1与足量金属钠反应可放出22.4氢气(标准状况)。
 请根据以上信息回答下列问题:
请根据以上信息回答下列问题:
 (1)的结构简式为(不考虑立体结构),由生成的反应类型是反应;
(1)的结构简式为(不考虑立体结构),由生成的反应类型是反应;
 (2)的结构简式为;
(2)的结构简式为;
 (3)由生成的化学方程式为,中官能团有(填名称),与具有相同官能团的的同分异构体还有(写出结构简式,不考虑立体结构);
(3)由生成的化学方程式为,中官能团有(填名称),与具有相同官能团的的同分异构体还有(写出结构简式,不考虑立体结构);
 (4)的结构简式为;
(4)的结构简式为;
 (5)由
(5)由 生成的化学方程式。
生成的化学方程式。
某探究小组利用丙酮的溴代反应
()来研究反应物浓度与反应速率的关系。反应速率通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:


 分析实验数据所得出的结论不正确的是()
分析实验数据所得出的结论不正确的是()
| A. |
增大增大 |
| B. |
实验②和③的相等 |
| C. |
增大增大 |
| D. |
增大,增大 |
下列关于有机物的说法错误的是()
| A. |
可由制得,可萃取碘水中的碘 |
| B. |
石油和天然气的主要成分都是碳氢化合物 |
| C. |
乙醇、乙酸和乙酸乙酯能用饱和溶液鉴别 |
| D. |
苯不能使溶液褪色,因此苯不能发生氧化反应 |
设为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 24 镁的原子量最外层电子数为 |
| B. | 1 0.1 乙酸溶液中 数为0.1 |
| C. | 1 甲烷分子所含质子数为10 |
| D. | 标准状况下,22.4 乙醇的分子数为 |
 光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为
光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为 ,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):


 (1)化合物II的分子式为。
(1)化合物II的分子式为。
 (2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);

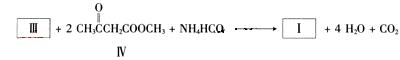
 化合物III的名称是。
化合物III的名称是。
 (3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为。
(3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为。


 (4)下列说法正确的是(填字母)
(4)下列说法正确的是(填字母)

| A. |
化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛

|
B. |
化合物I具有还原性;II具有氧化性,但能被酸性高锰酸钾溶液氧化

|
C. |
化合物I、II、IV都可发生水解反应

|
D. | 化合物V遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应 |
 (5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有种。
(5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有种。

下图中是一种具有水果香味的合成香料,是有直链有机物,与溶液作用显紫色。



请根据上述信息回答:
 (1)中含氧官能团的名称是。的反应类型为。
(1)中含氧官能团的名称是。的反应类型为。
 (2)只用一种试剂鉴别、、,该试剂是。
(2)只用一种试剂鉴别、、,该试剂是。
 (3)与互为同分异构体,在酸性条件下水解有乙酸生成,的结构简式为。
(3)与互为同分异构体,在酸性条件下水解有乙酸生成,的结构简式为。
 (4)和反应生成的化学方程式为。
(4)和反应生成的化学方程式为。
三聚氰胺(结构式如图9所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域。一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量。下列说法正确的是



| A. |
三聚氰胺是一种蛋白质

|
B. |
三聚氰胺是高分子化合物

|
C. |
三聚氰胺分子中含有碳碳双键

|
D. | 三聚氰胺的分子式为 |
有机物是最常用的食用油氧化剂,分子式为,可发生如下转化:



 已知的相对分子质量为60,分子中只含一个甲基。的结构可表示为:
已知的相对分子质量为60,分子中只含一个甲基。的结构可表示为:

 请回答下列问题:
请回答下列问题:
 (1)根据系统命名法,的名称为。
(1)根据系统命名法,的名称为。
 (2)官能团的名称为,高聚物的链节为。
(2)官能团的名称为,高聚物的链节为。
 (3)的结构简式为。
(3)的结构简式为。
 (4)反应⑤的化学方程式为。
(4)反应⑤的化学方程式为。
 (5)有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。
(5)有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。
 i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
 (6)从分子结构上看,具有抗氧化作用的主要原因是(填序号)。
(6)从分子结构上看,具有抗氧化作用的主要原因是(填序号)。
 a.含有苯环 b.含有羰基 c.含有酚羟基
a.含有苯环 b.含有羰基 c.含有酚羟基

 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号