辽宁省鞍山市高三第二次质量调查理综化学试卷
下列说法不正确的是
| A.开发利用太阳能与风能是发展低碳经济的重要途径 |
| B.地沟油对人体危害严重,查证没收后应燃烧处理 |
| C.氮化硅、碳化硅可做耐高温、耐磨材料 |
| D.氯气、臭氧、高铁酸钾都是常用的自来水消毒剂 |
饱和一元醇R(C5H12O)以银为催化剂进行催化氧化得醛M,再经过酸性KMnO4氧化最终得到羧酸N,则R与N最多可形成酯
| A.9种 | B.16种 | C.32种 | D.64种 |
下列离子方程式与实验事实相符且正确的是
| A.向AgI浊液中滴入NaCl溶液,产生大量白色沉淀:AgI(s) + Cl-(aq) =" AgCl(s)" + I-(aq) |
| B.用氨水除去铝片表面的氧化膜:Al2O3 + 2NH3·H2O = 2AlO2- + 2NH4+ + H2O |
| C.用铁氰化钾溶液检验Fe2+:3Fe2+ + 2[Fe(CN)6]3- = Fe3[Fe(CN)6]2↓ |
| D.向酸性KMnO4溶液中滴入过氧化氢产生无色气泡:2MnO4- + 9H2O2 + 6H+ = 2Mn2+ +7O2↑+ 12H2O |
X、Y、Z、W为四种短周期元素。已知X、Y的原子得到两个电子形成稀有气体原子结构时,X放出的能量大于Y。Z、W的原子失去一个电子形成稀有气体原子结构时,W吸收的能量大于Z。则下列关于四种元素的说法正确的是
| A.W、X两元素对应的单质发生反应只能得到W2X |
| B.由X、Y、Z三种元素组成的物质其水溶液一定呈中性 |
| C.1 mol Z2X2与足量水反应可得气体11.2 L |
| D.四种元素在自然界中均以化合态存在 |
色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中。纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是
| A.色氨酸的分子式为C11H12N2O2 |
| B.色氨酸能发生取代、加成、酯化、中和反应 |
| C.色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐 |
| D.将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽 |
将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是
| A.铁棒AB段发生反应为O2 + 4e- + 2H2O = 4OH- |
| B.腐蚀过程中在铁棒上会产生微电流,且方向是AB段到BC段 |
| C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响 |
| D.产生这种现象的本质原因是铁棒所处的化学环境不同 |
某二元酸H2A在水溶液中以下列方式进行电离:H2A=H++HA- HA- H++A2-
H++A2-
下列说法正确的是
A.室温时,NaHA溶液pH<7,是由于HA-的电离程度大于其水解程度
B.在0.1 mol/L的Na2A溶液中:c(A2-) + c(HA-) + c(H2A) =" 0.1" mol/L
C.在0.1 mol/L的NaHA溶液中,一定有:c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)
D.向两份等体积NaHA、Na2A的浓度比为1 : 1的混合溶液中分别加入适当浓度的盐酸与氢氧化钠,其pH随加入酸、碱量的变化图像为:

铁是人类目前使用最多的金属,可以形成多种氧化物。某实验小组欲利用氢气还原法测定某铁的氧化物(FexOy)的组成,根据实验内容回答下列问题:
I.定性分析:氧化物中铁元素的价态
(1)取适量该氧化物溶于过量的 (填“稀硫酸”、“稀盐酸”或“稀硝酸”),取少量溶液分别装入两支洁净的试管甲、乙中。甲试管中加入高锰酸钾溶液,乙试管中加入硫氰化钾溶液,能证明该氧化物中同时含有Fe2+、Fe3+的现象是: 。
II.定量分析:氧化物的组成
(2)按各部分仪器在该实验中的作用分析:装置E中盛放的药品是 ,作用是 。
(3)实验装置用上面所列仪器组成,按氢气流向的连接顺序是(括号中填入接口字母):
a→( )→( )→( )→( )→( )→( )→( )→( )→( )
(4)实验前,将该铁的氧化物放在坩埚内低温烘焙,这样做的目的是: ,若缺少此步骤,会导致x : y (填“偏大”、“偏小”或“无影响”)。
(5)称取烘焙后样品3.04 g,与氢气充分反应后生成水0.9 g,则该样品的组成为: 。
软锰矿的主要成分为MnO2,工业可用其按如下方法制备高锰酸钾:
a.将软锰矿初选后粉碎,与固体苛性钾混合,加入反应釜中敞口加热至熔融,并保持熔融状态下搅拌25~30 min,冷却得墨绿色熔渣(主要成分为K2MnO4);
b.将熔渣粉碎,加入去离子水溶解,充分搅拌后过滤得墨绿色滤液1;
c.取适量70%硫酸,加入滤液1中,边加边搅拌,直至不再产生棕褐色沉淀,过滤,得紫色滤液2;
d.提纯滤液2即可得高锰酸钾粗品。
根据上述内容回答下列问题:
(1)步骤a中,反应物熔融状态下搅拌的目的是: ,用化学方程式表示出MnO2转化为K2MnO4的反应原理: 。
(2)粉碎后的软锰矿与苛性钾置于 中进行加热。
A.陶瓷反应釜 B.石英反应釜 C.铁制反应釜
(3)写出步骤c中反应的离子方程式: 。
(4)步骤d中由滤液2得到高锰酸钾粗品的主要操作步骤是: 。
(5)若将母液循环使用,可能造成的问题是: 。
(6)早先有文献报道:步骤a中加入KClO3固体会缩短流程时间以及提高高锰酸钾的产率,但从绿色化学角度考虑后,现在工厂中一般不采用此法,你认为这种方法不符合绿色化学的原因是: 。
氯化硫酰(SO2Cl2)是一种无色液体,遇水剧烈水解,其熔点为-54.1 ℃,沸点为69.1 ℃,可用作氯化剂及锂电池正极活性物质。氯化硫酰可用下列反应制取:
SO2(g)+Cl2(g) SO2Cl2(l) △H=-97.3 kJ/mol。
SO2Cl2(l) △H=-97.3 kJ/mol。
(1)为了提高上述反应中Cl2的平衡转化率,下列措施合理的是(用字母编号填写): 。
a.缩小容器体积 b.使用催化剂 c.提高SO2浓度 d.提高温度
(2)300 ℃时,在体积为1 L的密闭容器中充入16.20 g SO2Cl2,达到平衡时容器中含SO2 7.616 g,则300 ℃时合成SO2Cl2反应的平衡常数的为: 。
(3)某同学设计了下图所示装置制取氯化硫酰:
①有关该装置的说法正确的是(用字母编号填写): 。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭起催化作用
c.B处反应管的冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U形管中盛放的可能是碱石灰
②从化学平衡的角度分析,反应管通冷却水的目的是: 。
③氯磺酸(ClSO3H)受热分解也可制得氯化硫酰,并得到另外一种物质,该反应的化学方程式为______,分离产物的方法是: 。
(4)下图为GET公司开发的Li-SO2Cl2军用电池的示意图。已知该电池的总反应为:2Li+SO2Cl2=2LiCl+SO2↑,则该电池工作时的正极反应为:_______________________。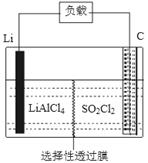
【化学——选修2 化学与技术】选考高炉炼铁是钢铁生产中的重要环节。这种方法是由古代竖炉炼铁发展、改进而成的。尽管世界各国研究发展了很多新的炼铁法,但由于高炉炼铁技术经济指标良好,工艺简单,生产量大,劳动生产率高,能耗低,这种方法生产的铁仍占世界铁总产量的95%以上。
(1)高炉炼铁的原料有铁矿、焦炭和石灰石,其中起熔剂作用的是 ,目的是除去铁矿石中的脉石,其产物密度比铁 ,所以在铁水的 (填“上部”或“下部”)形成炉渣而与铁水分离。
(2)焦炭在高炉炼铁中起着举足轻重的作用,下列不属于焦炭作用的是 。
| A.作为燃料,为炼铁中的化学反应提供能量 |
| B.作为还原剂与二氧化碳反应产生还原氧化铁的一氧化碳 |
| C.对高炉中的物料起到支撑和疏散的作用 |
| D.除去铁矿石中的杂质 |
(3)高炉炼铁的污染非常严重,目前我国部分大城市中的钢铁厂借着搬迁的机会也在进行着工艺改进。高炉炼铁导致的环境污染有 。
(4)写出以赤铁矿为原料进行高炉炼铁时与碳元素有关的氧化还原反应化学方程式: 。
【化学——选修3 物质结构与性质】选考下图为元素周期表的一部分,字母下方数值为该元素电负性,根据信息回答下列问题(用相应元素符号进行答题):
(1)b、h两元素可形成化合物bh2,写出其电子式: 。
(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为 ,eg3、e2g6中心原子e的杂化方式分别为 、 。
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式: 。
(4)f、g、h、i四种元素对应单质分子的键能如下表:
| 共价键 |
f—f |
g—g |
h—h |
i—i |
| 键能(kJ/mol) |
157 |
242.7 |
193.7 |
152.7 |
试从原子半径角度阐述f—f键键能反常的原因: 。
(5)c元素的元素符号是 ,价电子排布式为 ,下图是
一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图中勾画出该晶体的一个晶胞。计算出该合金的化学式为: 。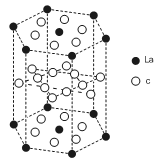
【化学——选修5 有机化学基础】选考化合物对MPMC主要用于化妆品中,作紫外吸收剂,同时也是众多药物的中间体原料。下图是其合成路线,根据内容回答问题:
已知:(i)A的分子式为C7H8O,核磁共振氢谱中四组峰,且不能与金属钠发生反应,B的苯环上一氯代物有2种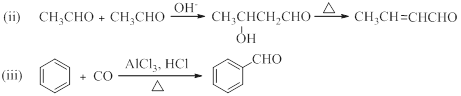
(1)写出下列化合物的结构简式:A ;D 。
(2)下列反应的类型属于② ,③ ,⑤ 。
(3)合成路线中加入④、⑥两步反应的意义是: 。
(4)写出⑦的反应方程式 。
(5)已知同一碳原子上连接两个单键氧原子的结构不稳定,则满足下列条件的B的同分异构体有 种,其中能发生银镜反应的有 种。
a.属于芳香化合物;
b.能发生酯化反应。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号