期中备考总动员高三化学模拟卷【新课标I卷】8
下列化合物中与自身类别相同的同分异构体数目(不考虑立体异构)最多的是
| A.戊烷 | B.戊醇 |
| C.戊烯 | D.乙酸丙酯 |
【改编】科学家从化肥厂生产的(NH4)2SO4中检出化学式为N4H4(SO4)2的物质,该物质的晶体中含有 和
和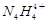 两种离子,当
两种离子,当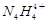 遇到碱性溶液时,会生成N4分子。下列说法正确的是
遇到碱性溶液时,会生成N4分子。下列说法正确的是
| A.N4与N2互为同位素 |
| B.N4H4(SO4)2为弱电解质 |
| C.N4H44+与NaOH溶液反应的离子方程式为N4H44++4OH-=N4+4H2O |
| D.N4H44+中只含有极性共价键,不含非极性共价键 |
标准状态下,气态分子断开l mol化学键的焓变称为键焓。已知H-H、H-O和O-O键的键焓ΔH分别为436 kJ/mol、463 kJ/mol和495kJ/mol。下列热化学方程式正确的是
A.H2O (g)= H2(g)+ O2(g); ΔH=" -485" kJ/mol O2(g); ΔH=" -485" kJ/mol |
B.H2O (g)=H2(g)+ O2(g); ΔH="=+485" kJ/mol O2(g); ΔH="=+485" kJ/mol |
| C.2H2(g)+ O2 (g)= 2H2O(g)ΔH =" +485" kJ/mol |
| D.2H2(g)+ O 2(g)=2H2O(g)ΔH =" -485" kJ/mol |
【改编】X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生右图所示变化,其中B和C均为10电子分子。下列说法不正确的是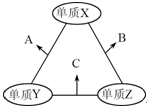
| A.Y元素位于VA族 |
| B.A与X的单质不能共存 |
| C.元素X与元素Z可形成1:1或1:2化合物 |
| D.A和C不可能发生氧化还原反应 |
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是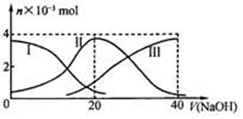
| A.当V(NaOH)=40mL时,c (Na+)+ c(H+)="2" c(A2-)+c(OH-) |
| B.当V(NaOH)=20mL时,溶液中离子浓度大小关系: c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D.HA-的电离程度小于水解程度 |
【原创】铁闸在海水中易被锈蚀,下图原理模型: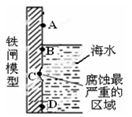
下列说法错误的是
| A.生成铁锈最多的是B点 |
| B.C处腐蚀时的电极反应为Fe-2e-=Fe2+ |
| C.以锌为负极,采用牺牲阳极法防止铁闸的腐蚀,可将锌放在C处。 |
| D.生锈最多的位置为腐蚀最严重的区域 |
利用下列实验装置进行的相应实验,不能达到实验目的的是
| A.用图1所示装置可制取氨气 |
| B.用图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| C.用图3所示装置可制取乙烯并验证其易被氧化 |
| D.用图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。
反应原理:
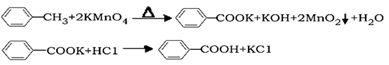
反应试剂、产物的物理常数:
| 名称 |
相对分子质量 |
性状 |
熔点 |
沸点 |
密度 |
溶解度 |
||
| 水 |
乙醇 |
乙醚 |
||||||
| 甲苯 |
92 |
无色液体易燃易挥发 |
-95 |
110.6 |
0.8669 |
不溶 |
易溶 |
易溶 |
| 苯甲酸 |
122 |
白色片状或针状晶体 |
122.4 |
248 |
1.2659 |
微溶 |
易溶 |
易溶 |
主要实验装置和流程如下:
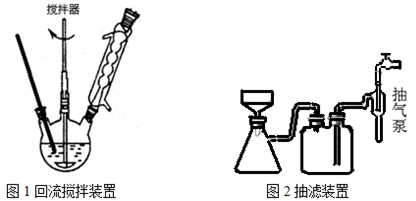
实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
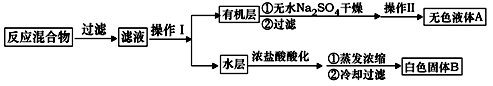
(1)无色液体A的结构简式为 。操作Ⅱ为 。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是 。
(3)下列关于仪器的组装或者使用正确的是 。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.图1回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入 ,分液,水层再加入 ,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为 。
硼及其化合物在耐髙温合金工业、催化剂制造、髙能燃料等方面应用广泛。
(1)氮化硼是一种耐高温材料,巳知相关反应的热化学方程式如下:
2B(s)+N2(g)=" 2BN(s)" ΔH="a" kJ • mol-1
B2H6 (g)="2B(s)" + 3H2 (g) ΔH ="b" kJ • mol-1
N2 (g) + 3H2 (g)  2NH3 (g) ΔH ="c" kJ• mol-1
2NH3 (g) ΔH ="c" kJ• mol-1
①反应B2H6(g)+2NH3(g)="2BN(s)" +6H2(g) ΔH = (用含a、b、c 的代数式表示)kJ ·mol-1。
②B2H6是一种髙能燃料,写出其与Cl2反应生成两种氯化物的化学方程式: 。
(2)硼的一些化合物的独特性质日益受到人们的关注。
①最近美国化学家杰西·萨巴蒂尼发现由碳化硼制作的绿色焰火比传统焰火(硝酸钡)更安全,碳化硼中硼的质量分数为78. 6%,则碳化硼的化学式为 。
②近年来人们将LiBH4和LiNH2球磨化合可形成新的化合物 Li3BN2H8和Li4BN3 H10,Li3BN2H8球磨是按物质的量之比n(LiNH2) : n(LiBH4) =" 2" : 1加热球磨形成的,反应过程中的X衍射图谱如图所示。

Li3BN2H8在大于250℃时分解的化学方程式为 ,Li3BN2H8与Li4BN3H10的物质的量相同时,充分分解,放出等量的H2,Li4BN3 H10分解时还会产生固体Li2NH和另一种气体,该气体是 。
(3)直接硼氢化物燃料电池的原理如图,负极的电极反应式为 。电池总反应的离子方程式为 。

【改编】雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

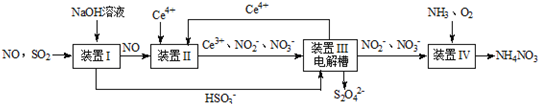
(1)装置Ⅰ的目的是 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。

①若是0.1molNaOH反应后的溶液,测得溶液的pH=4时,溶液中各离子浓度由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下反应的离子方程式 , 。
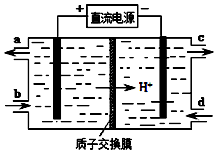
(4)装置Ⅲ中阴极反应方程式为 ;阳极使Ce4+再生,其原理如图所示。生成Ce4+从电解槽的 (填字母序号)口流出。
(5)若进入装置Ⅳ的溶液中的NO2-完全转化为NH4NO3,反应中氧化剂与还原剂的物质的量之比为 。
[化学——选修3:物质结构与性质]W、M、X、Y、Z是周期表前36号元素中的五种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质是大气污染物监测物之一;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)MX3-的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是___________________________。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
[化学——选修5:有机化学基础]肉桂酸甲酯是治疗白癜风的重要药物,也是一种用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2,其结构和性质如表所示:
| 结构 |
分子中只含有一个苯环,苯环上只有一个取代基且无支链,核磁共振氢谱图中有六个吸收峰,峰面积比为1∶2∶2∶1∶1∶3 |
| 性质 |
①能使溴水因发生化学反应而褪色 ②在NaOH溶液中易发生水解反应生成具有剧毒的醇类物质 |
试回答下列问题:
(1)肉桂酸甲酯的结构简式为________。
(2)用芳香烃A为原料合成肉桂酸甲酯G的路线如下:
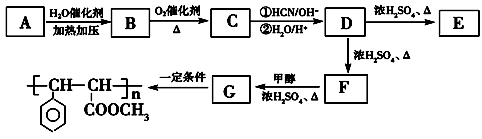
已知: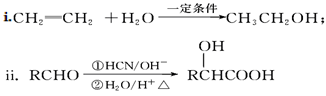
①B的结构简式为________,C中含有的官能团名称为________。
②D→F的反应类型是________;F→G的反应类型是________。
③D转化为F的化学方程式是______________________;
④E为含有三个六元环的酯,其结构简式是_____________________________。
⑤D分子中具有多种官能团,不能发生的反应类型有(填序号)________。
a.酯化反应
b.取代反应
c.加聚反应
d.水解反应
e.消去反应
f.氧化反应
⑥写出符合下列条件的D的同分异构体的结构简式______________________。
i.分子内含苯环,且苯环上只有一个支链;
ii.在催化剂作用下,1 mol该物质与足量氢气充分反应,最多消耗4 mol H2;
iii.它不能发生水解反应。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号