高考原创化学预测卷 04(山东卷)
化学与生活、社会、材料、能源关系密切,下列说法不正确的是
| A.人们常用漂粉精和明矾进行水的处理,二者的作用和反应原理不同 |
| B.航天服材质是由碳化硅/陶瓷和碳纤维等复合而成,它是一种新型无机非金属材料 |
| C.用于制作航空母舰上拦阻索的钢材是一种复合材料 |
| D.煤、沼气和液化石油气分别属于化石能源、可再生能源和二次能源 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.工业上采用电解法精炼铜,若阳极上溶解32gCu,则转移电子数目为NA |
| B.200mL 18mol·L-1浓硫酸与足量镁反应,转移电子数小于3.6NA |
| C.用含有0.5mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数小于0.5NA |
| D.0.1 mol羟基(-OH)与0.1mol OH‾所含电子数相同,均为NA |
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
| A.Y、Z、R与X形成的化合物的稳定性由强到弱的顺序是:Y > R > W |
| B.Z与Y形成的化合物能与H2SO4等强酸反应,属于碱性氧化物 |
| C.原子半径按X、Y、Z、R、W的顺序依次增大 |
| D.Z单质与W单质都能与稀硫酸和氢氧化钠溶液反应生成氢气 |
下表所列各组物质中,不能通过一步反应实现如图所示转化的是
| 选项 |
X |
Y |
Z |
| A |
AlCl3 |
Al(OH)3 |
NaAlO2 |
| B |
C |
CO |
CO2 |
| C |
CH2=CH2 |
CH3CH2Br |
CH3CH2OH |
| D |
S |
SO2 |
SO3 |
某有机物常用于制备液晶材料,结构简式为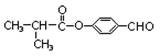 ,则下列说法正确的是
,则下列说法正确的是
| A.该有机物的分子式为C12H8O3 |
| B.该有机物可以发生水解反应、加成反应、氧化反应、还原反应 |
| C.该有机物的一溴代物有4种 |
| D.该物质属于芳香烃 |
下列说法不正确的是
A.恒温恒容容器中,发生反应C(s)+H2O(g) CO(g)+H2(g),当混合气体密度不变时反应达到平衡 CO(g)+H2(g),当混合气体密度不变时反应达到平衡 |
| B.平衡向右移动时,反应物的转化率一定增大,平衡常数不一定增大 |
| C.恒温时向BaSO4悬浊液中加入Na2SO4固体,混合后,Ba2+浓度减小,溶度积KsP (BaSO4)不变 |
| D.向氨水中逐滴加入盐酸,溶液呈中性时离子浓度为:c(Cl-)=c(NH4+)>c(H+)=c(OH-) |
(17分)合成氨技术的发明使工业化人工固氮成为现实。
(1)已知N2(g)+3H2(g)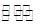 2NH3(g)
2NH3(g) 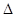 H=-92.2kJ·mol-1。在一定条件下反应时,当电子转移3mol时,放出的热量为 。
H=-92.2kJ·mol-1。在一定条件下反应时,当电子转移3mol时,放出的热量为 。
(2)合成氨混合体系在平衡状态时NH3的百分含量与温度的关系如下图所示。由图可知:
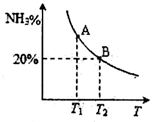
①温度T1、T2时的平衡常数分别为K1、K2,则K1 K2(填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,氮气的平衡转化率 (填“增大”、“减小”或“不变”)。
②T2温度时,在1L的密闭容器中加入2.1mol N2、l.5molH2,经10min达到平衡,则v(NH3)= 。达到平衡后,如果再向该容器内通入N2、H2、NH3各0.4mol,则V正 V逆(填“>”或“<” 或“=”)。
(3)工业上用CO2和NH3反应生成尿素:CO2(g)+2NH3(g) H2O(1)+CO(NH2)2(1) △H,
H2O(1)+CO(NH2)2(1) △H,
在一定压强下测得如下数据:
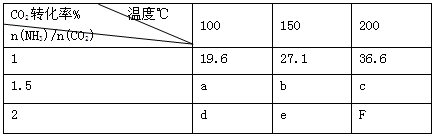
①该反应破坏旧化学键吸收的能量 形成新化学键放出的能量,表中数据a d,b f(均选填“>”、“=”或“<”)。
②从尿素合成塔内出来的气体中仍含有一定量的CO2、NH3,应如何处理 。
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。工业设计生产NaClO2的主要流程如下:

(1)气体b的化学式是 ,若装置III中生成49gA,则生成A的电极反应共 (填“失去”或“得到”)电子物质的量为 。
(2)I中反应的离子方程式是 。
(3)通电电解前,检验III中阴离子的方法和步骤是 。
(4)为防止II中制备的NaClO2被还原成NaCl,应选合适的还原剂,除双氧水外,还可以选择的还原剂
是 (填字母编号)。
a.Na2O2 b.FeCl2 c.Na2S
(5)常温时,HClO2的电离平衡常数Ka=1.07 10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中
10-2mol·L-1,II中反应所得NaClO2溶液(含少量NaOH)的pH=13,则溶液中 = 。
= 。
(6)气体a、b与氢氧化钠溶液可构成燃料电池,用该电池电解200 mL 0.5 mol·L-1的CuSO4溶液,生成铜3.2 g,此时所得溶液中离子浓度由大到小的顺序是 。
硫酸亚锡(SnSO4)、四氯化锡(SnCl4)常用于印染和电镀工业。
(1)某研究小组设计SnSO4制备路线如下:
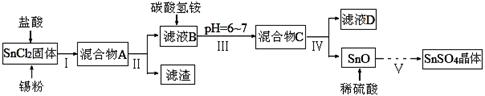
已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化;SnCl2极易水解。
①SnCl2酸溶后加入Sn粉的作用是 。
②步骤Ⅱ中用到的玻璃仪器除烧杯外还有 ;步骤Ⅳ中需要洗涤固体SnO中含有的杂质,检验SnO中的Cl-是否洗涤干净的操作为 。
③步骤Ⅴ涉及到的操作有:a.过滤 b.洗涤 c.蒸发浓缩 d.冷却结晶 e.低温干燥,则其正确的操作顺序为 。
(2)实验室拟用以下装置,用熔融的金属锡与干燥纯净的氯气制取无水SnCl4(SnCl4熔点-33℃,沸点114.1℃,遇潮湿空气极易水解),此反应过程放出大量的热。
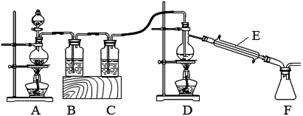
①装置C中应加入试剂为___________;仪器E的名称为____________________。
②反应开始生成SnCl4时,可以先熄灭___(填字母序号)处的酒精灯,理由是________。
③该实验装置设计尚存在缺陷,改进的方法是(包括仪器、试剂及连接位置等)______________。
【化学与技术】将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。
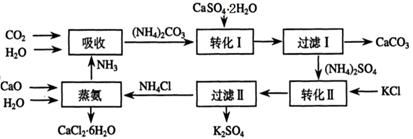
(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要______________等原料。
(2)石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式为_____________。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有 (填化学式)等物质,该固体可用作生产水泥的原料。
(4)检验过滤Ⅰ所得滤液中含有CO32-的方法是_____________________________。
(5)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________。
a.熔点较低(29℃熔化) b.能导电
c.能制冷 d.无毒
(6)上述工艺流程中体现绿色化学理念的是 。
【物质结构与性质】Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 |
Mn |
Fe |
|
| 电离能kJ/mol |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
|
回答下列问题:
(1)Mn元素核外电子的电子排布式为 ,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。其原因是 。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①Fe原子或离子易形成配合物的原因是 ,
与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 。
②络离子[Fe(CN)6]4-的配体CN-中C原子的杂化轨道类型是 ,HCN的分子构型为 ,写出一种与 CN-互为等电子体的单质分子的电子式 。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁的晶体构成微粒为 。
(4)金属铁晶体在不同的温度下有两种堆积方式,如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号