福建省泉州市高三上学期期末化学试卷
化学与生产、生活密切相关,下列说法不正确的是
| A.Al2O3熔点高,可用于制作耐高温仪器 |
| B.明矾净水与胶体的性质有关 |
| C.H7N9型禽流感病毒在高温条件下被杀死的过程是蛋白质变性 |
| D.高纯度的硅单质用于制作光导纤维,光导纤维有导电性 |
下列有关化学用语使用正确的是
A.氯原子的结构示意图: |
B.CO2分子的比例模型: |
C.具有10个中子的氧原子: |
| D.乙烯的结构简式:C2 H4 |
下列说法正确的是
A.14C、14N互为同位素
B.H2 O、CH3COOH、NH4 HCO3都属于电解质
C.铝、铁、铜对应的氧化物均为碱性氧化物
D.金属阳离子被还原时一定得到金属单质
下列关于有机化合物的说法正确的是
| A.糖类、油脂、蛋白质都属于天然高分子化合物 |
| B.分子式为C2 H6 O、C4 H10的有机物都有2种同分异构体 |
| C.乙烯和苯都能使酸性KMnO4溶液褪色 |
| D.可用热的NaOH溶液除去乙酸乙酯中的乙酸杂质 |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.1 mol OH一中含有9 NA个电子 |
| B.1 L 1 mol·L-1CH3 COONa溶液中含有NA个CH3 COO— |
| C.28g CO气体中含有NA个氧原子 |
| D.常温常压下11.2 L甲烷气体含有的分子数为0.5NA |
下列关于有机化合物的说法正确的是
| A.分馏产品是纯净物 | B.①主要发生物理变化 |
| C.②是石油的裂化 | D.③属于取代反应 |
短周期元素X、Y、Z在元素周期表中的相对位置如图所示,其中X原子最外层电子数是次外层电子数的3倍。下列说法错误的是
| A.元素X和元素Y的最高正化合价相同 |
| B.气态氢化物的热稳定性:H2 Y < H2 X |
| C.Y2 Z2是共价化合物 |
| D.酸性:HZO4 >H2YO4 |
常温下,下列各组离子在指定条件下可能大量共存的是
| A.弱碱性溶液中:Na+、K+、Cl一、HCO3一 |
| B.无色溶液中:Cu2+、K+、SO42一、NO3一 |
| C.pH=0的溶液中:ClO一、SO42一、Fe2+、K+ |
| D.由水电离的c(OH一)=10-14 mol·L一1的溶液中:CH3 COO一、SO42一、Na+、NH4+ |
下列方程式错误的是
A.0.1mol·L-1CH3 COOH溶液的pH为3:CH3 COOH H++CH3 COO— H++CH3 COO— |
| B.A1Cl3溶液中加入过量稀氨水:A13++3NH3·H2 O=A1(OH)3↓+3 NH4+ |
C.C12与过量的铁反应:3C12+2Fe 2FeCl3 2FeCl3 |
| D.NaHCO3溶液中加入稀盐酸:CO32一+2H+=CO2↑+H2 O |
反应CO2(g)+2NH3(g) CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
CO(NH2)2(s)+H2 O(g) △H<0,达到平衡时,下列说法正确的是
| A.加入催化剂,平衡常数不变 |
| B.减小容器体积,正、逆反应速率均减小 |
| C.增大CO(NH2)2的量,CO2的转化率减小 |
| D.降低温度,平衡向逆反应方向移动 |
用下图所示实验装置进行相应实验,能达到实验目的的是
| A.制氨气时,用装置①吸收尾气 |
| B.按装置②所示的气流方向收集NH3等 |
| C.用图③所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| D.用图④所示装置分离CCl4萃取碘水后的混合液 |
将反应Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
| A.KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B.Ag作负极,Cu作正极 |
| C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大 |
| D.取出盐桥后,电流计的指针依然发生偏转 |
下列实验结论正确的是
| A.向某溶液中加入稀盐酸,产生的气体通人澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定不含K+ |
| C.将某气体通人溴水中,溴水颜色褪去,该气体一定是SO2 |
| D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
下列溶液中,相关微粒的浓度关系正确的是
| A.MgSO4溶液:c(Mg2+)+c(H+)=" c" (SO42一)+c(OH一) |
| B.将0.2mol·L-1CH3 COOH溶液与0.1mo1·L-1NaOH溶液等体积混合:c(CH3 COO一)+ c(CH3COOH)=2c(Na+) |
| C.将pH=2的盐酸与0.01 mo1·L-1氨水等体积混合:c(NH4+)=" c" (Cl一) |
| D.由AgCl和AgI固体混合物与水形成的悬浊液:c(Ag+)>c(Cl一) =" c" (I一) |
下列物质性质与应用及其对应关系均正确的是
| 选项 |
性质 |
应用 |
| A |
碳酸氢钠可与烧碱反应 |
可用碳酸氢钠作糕点膨松剂 |
| B |
AgCl难溶于稀硝酸 |
可用稀硝酸和AgNO3溶液检测Cl一 |
| C |
浓硫酸具有强氧化性,而稀硫酸的氧化性较弱 |
可用浓硫酸替代稀硫酸与锌反应快速制氢气 |
| D |
碳单质性质稳定 |
可在纯铁中加入少量炭增强抗腐蚀性 |
下列有关实验的说法正确的是
| A.制氯气时,用饱和碳酸钠溶液和浓硫酸净化气体 |
| B.制少量氧化钠时,将钠置于纯氧中燃烧 |
| C.制二氧化硫时,用浓硫酸干燥气体 |
| D.配制氢氧化钠溶液时,称取一定质量氢氧化钠固体放人容量瓶中并加水至刻度线 |
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:
2K2FeO4+16HCl=4KCl+2FeCl3+8H2O+3Q↑,下列说法正确的是
| A.可用湿润的淀粉碘化钾试纸检验产物Q |
| B.K2FeO4在水中的电离方程式为K2FeO4=2K++Fe6++4O2一 |
| C.反应中氧化剂与还原剂的物质的量之比为1:8 |
| D.反应中涉及的6种物质均为电解质 |
LiAlH4由Li+、A1H4一构成,是有机合成中常用的还原剂。
(1)Al元素在周期表的位置是第__________周期__________族。
(2)比较离子半径大小:Li+__________ H一(选填“>"、“<”或“=”)。
(3)LiAlH4中含有的化学键类型为____________________________________。
(4)LiAlH4中氢元素的化合价为__________,它与水反应生成的单质气体为__________。
(5)LiCl溶液显酸性,用离子方程式说明原因____________________________________。
(6)如图所示,已知75%A的水溶液常用于医疗消毒,则A的结构简式为__________;CH3COOH与A在浓硫酸催化下生成B的有机反应类型为__________。
湿法炼锌为现代炼锌的主要方法,下列是以硫化锌精矿为原料制备单质锌的工业流程。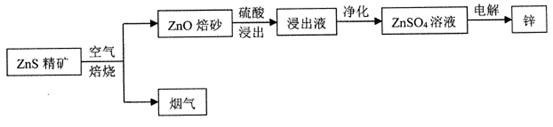
(1)烟气不能直接排放,可用于制取一种常见的强酸,该强酸为__________。
(2)浸出液以硫酸锌为主,还含有Fe3+、Fe2+、A13+、Cu2+、Cd2+、C1一等杂质,会影响锌的电解,必须除去。净化过程如下:
①在酸性条件下,用H2O2将Fe2+氧化成Fe3+,离子方程式为______________________。
②将浸出液的pH调节为5.5左右,使Fe3+、A13+形成沉淀而除去,可选用的试剂为_____(填字母)
| A.NaOH | B.NH3·H2 O | C.ZnO | D.H2 SO4 |
③用Zn除去Cu2+和Cd2+
④用Ag2SO4除去Cl一,发生的反应为Ag2SO4+2Cl一 2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。
2AgCl+ SO42-,室温下该反应的平衡常数K=_____________[已知室温下Ksp(Ag2SO4)="6.0x" 10-5,Ksp(AgCl)="2.0x" 10-10]。
(3)控制一定条件,用惰性电极电解硫酸锌溶液制取锌,锌在____极析出,阳极反应式为__________。
氢气是一种理想的“绿色能源”,下图为氢能产生与利用的途径
(1)上图中4个过程中能量转化形式有_____________
| A.2种 | B.3种 | C.4种 | D.4种以上 |
(2)电解过程要消耗大量电能,而使用微生物作催化剂在阳光下即可分解
2H2O(1) 2H2(g)+O2(g)△H1
2H2(g)+O2(g)△H1
2H2O(1) 2H2(g)+O2(g)△H2
2H2(g)+O2(g)△H2
以上反应的△H1_____________△H2 (选填“>"、“<”或“=”)

(3)已知H2 O(1)→H2 O(g)△H=" +44" mol·L-1,依据右图能量变化写出氢气燃烧生成液态水的热化学方程式________________________________。
(4)氢能利用需要选择合适的储氢材料
①镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) LaNi5H6(s) △H<0,欲使LaNi5H6 (s)释放出气态氢,根据平衡移动原理,可改变的条件之一是__________________。
LaNi5H6(s) △H<0,欲使LaNi5H6 (s)释放出气态氢,根据平衡移动原理,可改变的条件之一是__________________。
②一定条件下,如图所示装置可实现有机物的电化学储氢,总反应:2C7 H8+6 H2O(1) 2C7 H14+3O2 (g),电解过程中产生的气体X为_____,电极A发生的电极反应式为_________________。
2C7 H14+3O2 (g),电解过程中产生的气体X为_____,电极A发生的电极反应式为_________________。
根据物质相似性、特殊性来学习元素性质是常见的学习方法。
(1)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式_____,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2 BeO2+2H2 O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加人量的变化图:
(2)锗与硅元素相似,锗也是良好的半导体,以下是工业冶炼锗的简单流程图:
①GeCl4的晶体类型为__________。
②写出过程III发生反应的化学方程式__________。
③以下有关工业冶炼锗的说法正确的是__________。
| A.GeO2与SiO2性质相似,均易与盐酸反应 |
| B.过程II的蒸馏是利用GeCl4难溶于水的性质实现的 |
| C.过程IV发生的反应中,GeO2作氧化剂 |
| D.上述过程涉及的基本反应类型有复分解反应、置换反应 |
(3)某同学为了探究硫与浓硝酸的反应产物,将硫与浓硝酸混合,结果生成一种纯净无色气体A,A遇空气变红棕色,据此写出硫与浓硝酸反应的化学方程式___________________。
针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
活动一:查阅资料
NaNO2有毒,具有氧化性和还原性,NaNO2溶液显碱性,肉类在放置过程中,NaNO3逐渐转化为NaNO2,国家规定肉制品中NaNO2含量不能超过30mg/kg。
活动二:鉴别NaNO2与食盐
(1)NaNO2与食盐的外观相似,易被当成食盐误用,分析以下两种鉴别方法:
①能否各取少许固体用舌头品尝?____________。
②用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是NaNO2具有_________性。
活动三:探究NaNO3与NaNO2的相互转化
(2)制取NaNO2与NaNO3混合溶液的装置示意图如下
已知:2NO2+2NaOH=NaNO2+NaNO3+H2 O
①写出装置I中发生反应的化学方程式____________________________。
②水_____________(选填“能"或“不能”)作为装置II中的试剂,理由是_____________。
③装置III中反应完全后,接下来的操作是____________________________。
(3)将NaNO2与NaNO3混合溶液露置于空气,隔夜后,测得溶液的pH减小,则溶液中NaNO2的含量_____(选填“增多”、“减少"或“不变”),原因可能是____________________________(用化学方程式解释)。
活动四:检测熟肉中NaNO2含量的变化
(4)分别从1000g刚煮熟的肉和1000g隔夜熟肉中提取NaNO3与NaNO2后,配成溶液,再分别用0.00500mol/L的高锰酸钾(酸性)溶液滴定,刚煮熟的肉消耗12.00mL,隔夜肉消耗16.00mL,(已知:2MnO4一+5 NO2一+6H+=2 Mn2++5NO3一+3 H2 O)
①滴定终点的判断依据为________________________________________________。
②隔夜熟肉中NaNO2的含量是____________mg/kg。
活动五:综合其它实验和查阅资料获知,熟肉在细菌等作用下,NaNO3部分转化为NaNO2但只要保存得当,隔夜仍可食用。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号