湖北省襄阳市四校高一上学期期中联考化学试卷
下列生活中的现象与氧化还原反应知识有关的是
| A.食盐放在水中片刻后消失了 |
| B.食醋洒在大理石台面上产生气泡 |
| C.烧菜用过的铁锅,放置后常出现红棕色斑迹 |
| D.用食醋可以除去水壶中的水垢[水垢的主要成分为CaCO3、Mg(OH)2] |
下列仪器①蒸馏烧瓶②试管③蒸发皿④容量瓶⑤冷凝管⑥烧杯中能用酒精灯直接加热的是
| A.②③⑤ | B.②③ | C.①③④ | D.③⑤⑥ |
关于KOH溶液和Fe(OH)3胶体描述正确的是
| A.两者的分散质都属于碱 |
| B.两者均为有色不透明的分散系 |
| C.两者分散质的直径都介于10-9~10-7m之间 |
| D.两者都有丁达尔效应 |
量取10mL碘的饱和水溶液,倒入分液漏斗中,然后注入4mL四氯化碳,用力振荡后静置,实验现象为
| A.液体分层,上层为四氯化碳层,黄色 | B.液体分层,上层为水层,紫色 |
| C.液体分层,下层为四氯化碳层,紫色 | D.液体分层,下层为水层,黄色 |
下列实验操作中不正确的是
| A.用规格为10mL的量筒量取6.2mL的液体 |
| B.用蒸发方法使NaCl从溶液中析出时,应边加热边搅拌直至溶液完全蒸干 |
| C.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D.制取蒸馏水时,冷凝管中冷凝水应由下口进,上口出 |
标准状况下有①6.72LCH4②3.01×1023个HCl ③13.6gH2S ④0.2mol NH3下列对这四种气体的关系判断从小到大顺序不正确的是
| A.体积:④<①<②<③ | B.密度:①<④<③<② |
| C.质量:④<①<③<② | D.氢原子数:②<④<③<① |
在 xR2++ y H+ + O2="4" R3+ + n H2O的离子方程式中,下列判断正确的是
| A.y=4,R2+是氧化剂 | B.y=2,R2+是还原剂 |
| C.y=2,R3+是还原产物 | D.y=4,R3+是氧化产物 |
下列各组离子在无色水溶液中能大量共存的是
| A.Na+ Mg2+ Cl- OH- | B.MnO4-HCO3-OH- K+ |
| C.Fe3+H+ SO42-CH3COO- | D.K+ NO3- CO32- Na+ |
下图表示1gO2与1gX气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是
| A.N2 | B.CH4 | C.CO2 | D.NO |
下列溶液中溶质的物质的量浓度为1 mol/L的是
| A.将58.5g NaCl固体溶于1 L水中所得溶液 |
| B.将22.4L HCl气体溶于水配成1 L的溶液 |
| C.从1L 10mol/L的浓盐酸中取出的100mL溶液 |
| D.将4g NaOH固体溶于水中配成的100 mL溶液 |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,含有NA个氦原子的氦气的体积约为11.2L |
| B.标准状况下,44.8L H2O的分子数为2NA |
| C.常温常压下,22g CO2含有原子总数为1.5NA |
| D.含有1mol HCl 的稀盐酸与足量的铁发生反应,转移的电子总数为2NA |
下列反应对应的离子方程式书写正确的是
| A.盐酸与氨水反应 H++OH- ==H2O |
| B.硫酸铜溶液中滴加氢氧化钡溶液 Ba2++2OH-+Cu2++SO42-==BaSO4↓+Cu(OH)2↓ |
| C.硝酸银溶液中加入铜粉 Ag++Cu==Cu2++Ag |
| D.铁与稀盐酸反应 2Fe+6H+==2Fe3++3H2↑ |
下列检验方法和结论都正确的是
| A.加入AgNO3溶液有白色沉淀生成,证明原溶液中一定有大量Cl- |
| B.加入硝酸后的溶液中,滴加BaCl2溶液,有白色沉淀生成,证明原溶液中一定有大量SO42- |
| C.加入盐酸后,放出能使澄清石灰水变浑浊的无色气体,证明原溶液中一定含有大量CO32- |
| D.加入无色酚酞试液后,溶液显红色,证明原溶液中一定含有大量OH- |
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4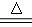 2ClO2↑+K2SO4+2CO2↑+2H2O (方程式中H为+1价,O为-2价)下列说法正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O (方程式中H为+1价,O为-2价)下列说法正确的是
| A.KClO3在反应中失电子 | B.ClO2是氧化产物 |
| C.H2C2O4在反应中被氧化 | D.1 molKClO3参加反应有2mol电子转移 |
质量分数为a%,物质的量浓度为c mol·L-1的NaCl溶液,蒸发溶剂,恢复到原来的温度,若物质的量浓度变为2c mol·L-1,则质量分数变为(蒸发过程中没有晶体析出,且NaCl溶液的密度大于1g/mL)
| A.等于2a% | B.大于2a% | C.小于2a% | D.无法确定 |
(10分)(1)在KCl和CaCl2的混合物中,K+和Ca2+的物质的量之比为2:1,则KCl和CaCl2的物质的量之比为 ,若要取出含1mol Cl-的该混合物,应称取该混合物的质量为 g。
(2)同温、同压下某瓶充满O2时重106克,充满CO2时重112克,充满某气体时重98克。则某气体的相对分子质量为 。
(3)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
在该反应中,若消耗了32 g Cu,则转移了_ __mol 电子 ,生成 _ _L SO2(标准状况)气体。
(8分)某无色透明溶液里加入紫色石蕊试液,溶液变红色,经分析该溶液中只可能存在下列离子:H+、Ba2+、Na+、Cu2+、OH-、SO42- ,
(1)请确定这些离子在该溶液中的存在情况:
一定存在的离子是 ;可能存在的离子是 ;
一定不存在的离子是 ;
(2)用离子方程式表示其中一种离子不能存在的原因 。
(15分) 现用98%浓硫酸(密度1.84g/mL)配制100mL1mol/L的稀硫酸。可供选用的仪器有:
①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒。请回答下列问题:
(1)保存浓硫酸的试剂瓶上除贴B标签外,还需贴上的标签是___________。
(2)配制稀硫酸时,上述仪器中不需要使用的有 (选填序号),还缺少的仪器有 ,使用之前首先必须进行 。
(3)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL。
(4)稀释时,一定要将 沿器壁慢慢倒入 中并不断搅拌.
(5)下列情况对所配制的稀硫酸浓度有何影响?(填写“偏大”、“偏小”、“无影响”)
| A.所用的浓硫酸长时间放置在密封不好的容器中 |
| B.容量瓶用蒸馏水洗涤后残留有少量的水 |
| C.转移溶液后,未洗涤烧杯和玻璃棒就直接定容 |
| D.定容时俯视溶液的凹液面 |
E.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(12分)为除去粗盐中的Ca2+、Mg2++、SO42+以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)步聚⑤步实验操作需要的玻璃仪器有烧杯、_____ ____、__ ___ 。
(2)步聚④步中,相关的离子方程式是 、 。
(3)步聚②中,判断加入BaCl2已过量的方法是: 。
(4)除杂试剂Na2CO3、NaOH、BaCl2加入的先后顺序还可以是(用化学式填写,只填一种情况 )
→ →
(5)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是(请写出其中一个离子方程式) 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号