浙江省温州市十校联合体高一上学期期中联考化学试卷
1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是
| A.化学不再是纯实验科学 | B.化学不再需要实验 |
| C.化学不做实验,就什么都不知道 | D.未来化学的方向还是经验化 |
下列各组物质中,肯定全都属于纯净物的是
| A.液氯和氯水 | B.酒精溶液和乙醇 |
| C.七水合硫酸亚铁和硫酸亚铁 | D.干冰和盐酸 |
下列说法不正确的是
| A.过氧化钠可以作为漂白剂和供氧剂 |
| B.用二氧化氯取代氯气对饮用水消毒更好 |
| C.侯氏制碱法是以氯化钠等为原料制取烧碱的工业生产 |
| D.碳酸氢钠是用于治疗胃酸过多的一种药剂 |
对于相同物质的量的SO2和SO3,下列说法中正确的是
| A.氧元素的质量比为1∶1 | B.质量之比为1∶1 |
| C.原子总数之比为1∶1 | D.分子数之比为1∶1 |
下列物质按一定的分类方法属于同一类的是
| A.标准状况下的状态:O2、N2、NO、H2O | B.酸性氧化物:CO2、SO2、Cl2O7、N2O5 |
| C.非电解质:酒精、蔗糖、葡萄糖、醋酸 | D.混合物:液氯、盐酸、漂白粉、氯水 |
某盐的混合物中含有0.2mol Na+,0.4mol Mg2+,0.4mol Cl-,则SO42-为
| A.0.1mol | B.0.5mol | C.0.3mol | D.0.15mol |
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B.25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C.在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| D.在标准状况下,11.2L H2O含有的分子数为0.5NA |
下列关于胶体的叙述不正确的是
| A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间 |
| B.光线透过胶体时,胶体中可发生丁达尔效应 |
| C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
| D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
与100mL 0.5mol·L-1NaCl溶液中的Cl-的物质的量浓度相同的是
| A.100mL 0.5 mol·L-1MgCl2溶液 |
| B.100mL 0.5mol·L-1HCl溶液 |
| C.200mL 0.25 mo l·L-1 KCl溶液 |
| D.100mL 0.5mol·L-1NaClO溶液 |
设NA为阿伏加德罗常数,如果ag某气体含分子数为P,则bg该气体在标准状况下的体积V(L)是
A. |
B. |
C. |
D. |
下面有关Na2CO3与NaHCO3的性质比较中错误的是
| A.相同浓度溶液的pH:Na2CO3>NaHCO3 |
| B.在水中的溶解度:Na2CO3>NaHCO3 |
| C.与同浓度的硫酸反应放出气泡的速率:NaHCO3<Na2CO3 |
| D.热稳定性:NaHCO3<Na2CO3 |
下列反应的离子方程式书写正确的是
| A.稀硫酸滴在铜片上:Cu + 2H+ |
| B.氢氧化镁溶于盐酸:OH-+H+ |
| C.铁跟稀硫酸反应:2Fe+6H+ |
| D.铜和硝酸银溶液反应: Cu + 2Ag+ |
下列分离方法中不正确的是
| A.利用萃取方法用四氯化碳提取溴水中的溴单质 |
| B.利用蒸馏的方法可以分离沸点相差较大的液体混合物 |
| C.利用结晶的方法除去KNO3中的氯化钠 |
| D.利用分液的方法分离酒精和水 |
一种试剂就能鉴别出NH4Cl、Na2SO4、(NH4)2CO3三种溶液,应选用
| A.BaCl2 | B.HCl | C.NaOH | D.Ba(OH)2 |
对于反应3Cl2+6NaOH==5NaCl+NaClO3+3H2O,以下叙述正确的是
| A.Cl2是氧化剂,NaOH是还原剂 |
| B.被氧化的Cl原子和被还原的Cl原子的物质的量之比为5∶1 |
| C.Cl2既做氧化剂又做还原剂 |
| D.氧化剂得电子数与还原剂失电子数之比为5∶1 |
含有NaBr、NaI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是
| A.NaCl | B.NaCl和NaBr |
| C.NaCl和NaI | D.NaCl和I2 |
下列强酸性溶液中,能大量共存的是
| A.Ca2+、K+、HCO3-、OH- | B.Fe2+、Cl-、H+、MnO4- |
| C.Fe2+、Mg2+、Cl-、NO3- | D.K+、NH4+、SO42-、Cl- |
溴化碘(IBr)的化学性质与卤素单质相似,能跟大多数金属反应生成金属卤化物,能跟水反应IBr+H2O==HBr+HIO.下列有关叙述中不正确的是
| A.IBr是双原子分子 |
| B.IBr与水反应时,它既是氧化剂,又是还原剂 |
| C.在很多化学反应中IBr作氧化剂 |
| D.跟NaOH溶液反应可生成NaBr和NaIO |
下列物质:
①H2O ②石墨 ③NH4NO3 ④AgCl ⑤CH3COOH ⑥硫酸 ⑦NH3·H2O ⑧蔗糖,
其中属于强电解质的是 ;属于弱电解质的是 ;
属于非电解质的是 (用编号填写)
实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑ +8H2O
(1)该反应中的还原剂是 ,氧化产物是
(2)氧化剂与还原剂之比是
(3)如反应中转移了0.6mol电子,则产生的气体在标准状况下体积为
同温同压下的氮气和氢气,若体积相同时,两种气体的质量比为___________,其密度比为___________;若质量相等时,两种气体的体积比___________。
有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的1/2,乙元素原子核内无中子,丙元素原子核内有8个质子。
(1)写出乙、丙两种元素形成的两种化合物的化学式 ,
(2)写出甲、乙、丙三种元素组成的化合物在水中的电离方程式
(3)画出甲元素的原子结构示意图和丙离子的结构示意图 ,
二氯化硫(SCl2)熔点-78℃,沸点59℃。密度1.638 g·cm-3,遇水易分解,是一种重要的化工试剂,下图是氯气与硫在50~59℃时合成二氯化硫的实验装置。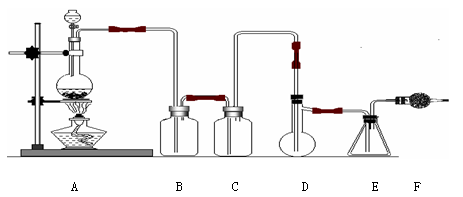
(1)装置A中发生反应的化学方程式为: 。
(2)装置B盛放的药品是 ,作用是 ;装置C盛放的药品是 ,作用是 。
(3)实验开始前先在D中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁表面形成一薄层,这样做的目的是 。
(4)F装置中干燥管内所盛物质是 ,一个作用是 ,还有一个作用是 。
2.3g钠溶于水中形成溶液,所得溶液中Na+和H2O的个数比为1:100,则最初需要加入 克水。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号